Monteris修改脑消融装置以应对安全风险
美国食品和药物管理局已经批准了Monteris Medical NeuroBlate探针的修改版本,旨在消除引发I类召回的意外发热问题并对脑组织造成可能的风险。
该机构在收到可能由温度读数不准确引起的不良事件报告后,今年早些时候向医疗保健专业人员发出了与神经外科消融设备有关的危险信息以及Medtronic的竞争产品。
Monteris通过用非金属光纤传感器替换其原始设备中的金属热电偶温度传感器来应对意外加热的情况。
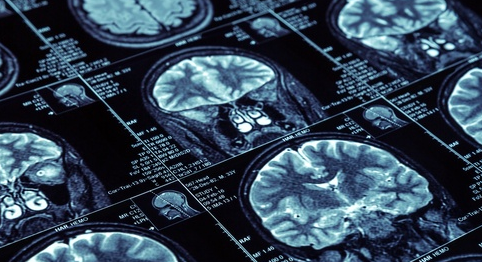
磁共振引导激光间质热疗是一种微妙的手术,可以在难以治疗的人群中产生积极的结果,例如某些形式的脑癌患者。将激光探针放入需要消融的肿瘤或其他组织中。一旦到位,激光就会释放能量来加热并杀死目标组织,同时外科医生会实时监测其效果。
4月,FDA报告对外科医生用于监测手术的磁共振测温读数的准确性表示怀疑。FDA关注的是图像分辨率和捕获时间等参数导致读数不准确,并且设备未能考虑到即使目标区域冷却,热能仍可继续扩散到周围组织的事实。
Monteris重新设计了其设备以应对这些担忧。FDA批准了修改后设备的上市前提交,并建议医疗保健专业人员与Monteris联系,以了解它何时可用。
与此同时,FDA希望医疗服务提供者在使用旧金属探针之前考虑风险和替代方案。美国食品和药物管理局周四重申其4月份发布的建议,旨在通过限制最高温度和采取其他预防措施来降低危害的风险。
FDA还向Medtronic的Visualase热疗系统用户提供建议。美敦力于6月份开始召回该设备,并在今年夏天向医疗保健专业人员发送了三封咨询信。这些信件详细说明了减轻该系统所带来风险的策略,Medtronic在2014年以1.05亿美元现金收购Visualase后收购了该系统。
Visualase在该机构签署Monteris竞争对手设备之前获得了FDA批准,并且在过去几年中受益于Medtronic的营销力量。这与蒙特利斯的赔率相差甚远,但最近召回引发的修订使其在争夺市场份额方面有了新的视角。Monteris现在强调其使用光纤作为差异化因素。
推荐内容
-
5月7日邯郸要闻快报:最新!邯郸0新增!两地开展预防性核酸检测!一地
5月7日邯郸要闻快报:最新!邯郸0新增!两地开展预防性核酸检测!一地发布寻人公告 1、河北省卫健委最新通报2022年5月6日024时,河北省无
-
无线耳机致癌?该信吗?
日常生活中我们经常会听到各种各样的坊间流言。然而很少人去求证这些流言的真实性,久而久之就变成了真事。在这里,小编必须提醒大家,...
-
上海农业复产率逾93% 将创新蔬果产销对接方式
上海农业复产率逾93% 将创新蔬果产销对接方式 (上海战疫录)上海农业复产率逾93% 将创新蔬果产销对接方式 中新网上海5月4日电 (记者
-
洋葱防癌、降三高,是可以吃的心脏支架?生吃还是熟吃好?
洋葱防癌、降三高,是可以吃的心脏支架?生吃还是熟吃好? “洋葱是抗癌之王,多吃能杀死癌细胞!”“洋葱是蔬菜皇后,能防癌,还...
-
喝了这么多年板蓝根,其实它并不能预防感冒?很多人想问
日常生活中我们经常会听到各种各样的坊间流言。然而很少人去求证这些流言的真实性,久而久之就变成了真事。在这里,小编必须提醒大家,...
-
长清区经十西路:九如城长清康养中心
长清区经十西路:九如城长清康养中心 九如城长清康养中位于长清区城南经十西路路西20179号。项目占地面积约40亩,总床位436张。设立颐


