基因驱动不仅适用于昆虫 也适用于哺乳动物
如果村民们能够使用基因驱动技术,哈默林花衣魔笛手带来的所有麻烦都是可以避免的。直到最近,我们也没有这种技术。此外,它还被限制在对昆虫遗传的控制上。但是现在,由于加州大学圣地亚哥分校的工作,基因驱动可能很快就会促进基础和生物医学研究中更好的动物模型的发展。它甚至可能最终被用于抑制野外失控的啮齿动物种群,或者可能被用于晚期Hamelins的定居地区。
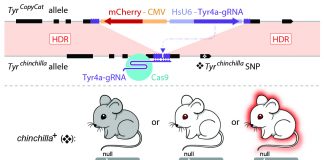
助理教授Kimberly Cooper说:“我们的动机是开发一种(基因驱动的)形式,作为实验室研究人员控制小鼠多基因遗传的工具。”“随着进一步的发展,我们认为将有可能制造出复杂的人类遗传疾病的动物模型,比如关节炎和癌症,这在目前是不可能的。”
基因驱动是一种编辑基因组的“主动遗传学”方法。它可以用来控制一个基因的两个副本中哪个传给下一代。
为了给老鼠带来基因驱动,库珀领导的一个研究小组设计了一种活跃的基因“模仿者”DNA元素,这种元素控制着皮毛的颜色。当模仿者干扰老鼠体内基因的两个副本时,原本是黑色的皮毛就会变成白色,这显然是他们研究成功的标志。
值得注意的是,模仿者元素也被设计成不能单独在人群中传播。换句话说,模仿者的设计是为了有效地将基因驱动带入公园。
1月23日,《自然》杂志发表了一篇题为《雌性小鼠生殖系中CRISPR-Cas9介导的超孟德尔遗传》的文章,详细介绍了模仿行为。这篇文章描述了研究人员如何使用一种活跃的遗传元素来编码一种嵌入在小鼠酪氨酸酶(Tyr)基因中的指导RNA,以评估当CRISPR-Cas9在早期胚胎或正在发育的生殖系中处于活跃状态时,是否会发生靶向基因转换。
“我们对8种不同基因策略的比较表明,与昆虫相比,当内源性减数分裂重组机制能够有效修复突变时,Cas9表达的精确时间对啮齿类动物来说可能是一个更大的挑战,即将DSB的形成限制在一个窗口内,”作者报告说。“尽管如此,我们在这里观察到的复制效率对于广泛的实验室应用来说已经足够了。”
“例如,使用最有效的遗传策略的女性中,观察到的44%的平均复制率结合了超紧密联系的酪氨酸酶突变,以至于22.5%的后代遗传了带有两个等位基因的染色体,这在孟德尔遗传中是不可能的。”
这种新方法在雌性小鼠产蛋期间有效,但在雄性小鼠产精期间无效。这可能是由于男性和女性减数分裂的时间不同,这一过程通常对染色体洗脱基因组,并可能有助于这一工程复制事件。
据加州大学圣地亚哥分校教授伊桑·比尔(Ethan Bier)说,该研究结果“为合成生物学的各种应用开辟了道路,包括研究不同生物过程的复杂遗传系统的模块化组装。”
库珀和她实验室的成员们现在正着手研究这第一个基于单一基因的活跃的哺乳动物遗传成功,并试图将这一工具扩展到多个基因和特征。
“我们已经证明我们可以将一种基因型从杂合子转化为纯合子。现在我们想看看我们是否能有效地控制动物体内三种基因的遗传。如果这项技术可以同时应用于多个基因,那么它将彻底改变老鼠的遗传学。
尽管这项新技术是为实验室研究开发的,但一些人设想,未来的基因驱动将以这种方法为基础,在野生环境中努力恢复包括啮齿动物在内的入侵物种泛滥的生态系统中自然生物多样性的平衡。
Bier说:“通过进一步的改进,应该有可能开发基因驱动技术来改变或可能减少作为疾病传播媒介的哺乳动物的数量,或对土著物种造成损害。”
然而,这些数据也表明,在野外实际使用需要技术改进,因此有时间仔细考虑可以而且应该实施这种新技术的哪些应用。然而,研究人员指出,他们的研究结果显示出了一项重大进展,可能已经减少了推进人类疾病的生物医学研究以及了解其他复杂遗传特征所需的时间、成本和动物数量。
“我们也对理解进化机制感兴趣,”库珀说。“例如,对于经过数千万年进化的某些特征,基因变化的数量比我们目前在老鼠身上收集到的要多,我们无法理解是什么导致蝙蝠的手指长出翅膀。”所以我们想要制造出许多活跃的基因工具来了解哺乳动物多样性的起源。
推荐内容
-
辟谣|肿瘤的治疗方法只有化疗? 还真不一定!
辟谣|肿瘤的治疗方法只有化疗? 还真不一定!全民自媒体时代,信息被大众获取的途径多种多样,但也出现了很多不实消息被误传的情况。所以
-
酵母菌株为来自乳糖的低热量甜味剂提供制造提升
寻求满足甜食而不增加腰围在其武器库中有一种新的武器:一种能够将乳糖(乳制品中的糖)代谢成塔格糖的酵母菌株,一种天然甜味剂,其中不...
-
高温来袭2019真的是"厄尔尼诺年"吗? 还真不一定!
高温来袭2019真的是"厄尔尼诺年"吗? 还真不一定!流量为王的时代,信息传播速度越来越快,但其中很多消息还没被证实真实性就大范围传...
-
阿尔茨海默病可能与传播疾病的缺陷脑细胞有关
罗格斯大学科学家表示,像阿尔茨海默氏症和帕金森氏症这样的神经退行性疾病可能与有缺陷的脑细胞有关,这些脑细胞处理使相邻细胞生病的...
-
笑出眼泪!石家庄一小区居民夜晚隔空玩“抓鸭子” 对话内容超好笑
笑出眼泪!石家庄一小区居民夜晚隔空玩抓鸭子 对话内容超好笑。近日,石家庄一小区居民夜间隔空玩起了抓鸭子游戏,一名居民大喊抓鸭子,立
-
Dolomite Bio推出用于单细胞研究的新型Nadia产品系列
Dolomite Bio很高兴宣布推出改变游戏规则的Nadia单细胞平台,这是一个突破性的系统,可将scRNA-Seq升级到新的高度,为快速增长的单细胞研
-
人体关节要省着点用吗? 这才是事实!
人体关节要省着点用吗? 这才是事实!随着传播途径的多样化发展,讯息传播效率飞速提高,但也出现了很多不实消息被误传的情况。因此我们在