干细胞重编程因子控制细胞能量产生的变化
筑波大学领导的研究人员探索了重编程因子KLF4在诱导多能干细胞(iPSCs)生产中的作用。显示KLF4结合Tcl1靶基因的上游,其控制细胞多能性获得期间能量产生的代谢变化。这有助于解释细胞如何将发育时钟从成人细胞转回干细胞,并且可以利用它来提高效率或限制iPSC生成期间的遗传损伤。
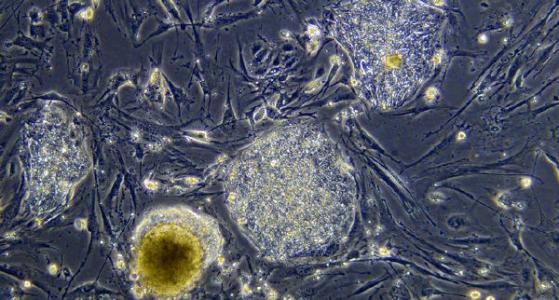
10多年前,成熟细胞首次重编程为未分化的干细胞。这些诱导多能干细胞(iPSCs)具有几乎任何细胞类型的能力,并且可以无限分裂,因此与胚胎干细胞共享许多特征。这些特征使iPSC能够用于再生医学的几种应用,特别是因为它们可以来自个体自身的细胞,因此不会遇到组织排斥问题。它们还可以被编程为发展成稀有或难以接近的细胞类型,用于筛选新药,并研究以了解疾病的细胞基础或重编程。
然而,尽管负责重编程的遗传因子是众所周知的,但诱导基因表达变化的反应机制尚不清楚。
现在,由筑波大学领导的研究解决了围绕其中一个重编程因子KLF4的谜团。该研究发表在干细胞报告中。
KLF4与其他重编程转录因子一起用于实验室中以迫使体细胞(成体非种系细胞)中的基因在iPSC的发育中表达。体细胞在称为氧化磷酸化的氧气燃烧过程中产生能量,氧化磷酸化发生在线粒体中,也称为细胞发电站。
相比之下,干细胞具有小的线粒体,并使用糖酵解作为产生能量的替代生化途径。这一系列反应可以是厌氧的,因此更适合于它们通常的低氧环境,但也提供快速生长和分裂所必需的代谢中间体的供应。
筑波大学的研究人员开发了一种基因转移系统,该系统允许iPSC重编程仅在KLF4存在的情况下发生,因此专注于其在该过程中的作用。然后,他们使用全基因组分析来搜索KLF4在重编程后期开启的基因。“我们发现Tcl1基因被KLF4与其增强子和启动子区域的结合上调,”研究共同第一作者Ken Nishimura说。“KLF4还导致另一种重编程因子OCT4与Tcl1启动子的结合。”
研究小组发现,TCL1蛋白通过激活对干细胞自我更新非常重要的不同代谢途径,在增加糖酵解中发挥了关键作用。“我们还发现TCL1抑制氧化磷酸化所需的线粒体酶,导致细胞耗氧量降低”,共同作者Shiho Aizawa解释说。“这与糖酵解的葡萄糖摄取增加相匹配,揭示了TCL1促进细胞获得多能性所必需的能量生成中的代谢转换。”
推荐内容
-
少吃饭能饿死肿瘤? 真实情况如何?
少吃饭能饿死肿瘤? 真实情况如何?随着互联网时代的到来,信息传播速度越来越快,但其中很多消息还没被证实真实性就大范围传播开了。因此
-
基因发现可能会阻止全球小麦的流行
加利福尼亚大学戴维斯分校的研究人员发现了一种能够抵抗新的破坏性茎锈病的基因,这种真菌病阻碍了整个非洲和亚洲的小麦生产,并威胁着...
-
方便面32小时不消化?事实又是什么?
随着互联网的快速发展,我们在获取信息的时候很容易被带跑方向。有时候真相也许并不是网上说的那样,所以我们必须要有自己的判断和独立...
-
12月4日广东广州疫情数据公布 广东昨日新增本土确诊1例
广东12月3日新增本土确诊1例 来自广州。那么,对于广州疫情的这个话题,今天的你是否也在关注着?具体什么情况?下面跟小编一起来了解下。12
-
虎骨头 狮子骨头 几乎绝种的苏铁 在入境口岸进行现场DNA检查
野生动物贩运者尽力使动物和植物部分无法辨认。当海关官员发现骨头时,也许他们可以说,骨头属于大型猫科动物。然后他们不得不问:那些...
-
冰淇淋融化后再冷冻有毒吗?该信吗?
当我们不知道一件事真假的时候,不防多等等官方的回应。因为信息碎片化,很多小伙伴现在上网很容易只看到事情的一面就下定论,其实很多...





