rna蛋白质网络或许可以解释为什么会长黑色素瘤
五年存活率是30%左右患者远处转移性疾病,皮肤黑素瘤是皮肤癌症相关死亡的主要原因。的黑色素瘤患者的存活率低的主要原因是病人的有限数量的选择缺乏BRAF突变和内在和获得性耐药现有疗法。所以有必要发展新的治疗策略来消除耐药细胞和/或目标患者不论他们的司机突变。
KU鲁汶为首的科学家合作,比利时,与东京大学农业和技术(TUAT),日本,揭示了一种新的方式来对抗黑色素瘤。他们报告melanoma-specific长非编码RNA,名叫SAMMSON,与蛋白质交互CARF妥善协调蛋白质合成细胞溶质和黑色素瘤细胞的线粒体。这种机制确保维护proteostasis在细胞生长,从而避免细胞死亡的感应。
“我们发现了一个名叫SAMMSON长非编码RNA表达在绝大多数(> 90%)的黑色素瘤患者,从未发现在正常成人组织,”艾Leucci博士说,文章的第二作者,LKI鲁汶癌症研究所,KU鲁汶。“在黑色素瘤,SAMMSON对适当的定位至关重要的蛋白质第9 -进入线粒体,它是核糖体生物起源和蛋白质合成所必需的。”
“我们报道,核浆蛋白质CARF礼物,间接减少了核糖体合成的核仁通过直接绑定到另一个蛋白质XRN2,”合著者Hideaki石川博士说,农业部TUAT,东京,日本。“在核仁,XRN2充当一种增加了核糖体合成的酶。但其活动和本地化由CARF的绑定使XRN2远离核仁。”
这些独立观察,连接后的第一作者MSc罗伯托·Vendramin发现SAMMSON CARF结合。这个观察引发了国际合作,导致工作发表在《自然结构和分子生物学》杂志上。
“我们发现,在黑色素瘤,部分CARF隔离到细胞质SAMMSON-dependent方式与第9 -”艾Leucci博士说。
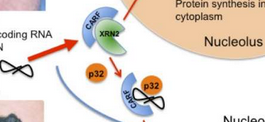
“释放CARF绑定,XRN2把从核浆核仁促进核糖体生物起源。一致的复杂CARF-SAMMSON-p32,转移到线粒体和促进线粒体核糖体合成。”
“我们得出结论,在黑素瘤细胞,SAMMSON增加了细胞核和线粒体核糖体合成一致,“Leucci博士说。“细胞有一个机制来感觉异常,如果核糖体合成在核仁或线粒体改变,并诱导细胞死亡。然而,当这个过程是在两个隔间改变细胞无法认识到的侮辱。因此,通过黑客一致核糖体生物起源机械、SAMMSON使细胞对损伤和促进黑色素瘤细胞生长”因此,一种物质,抑制SAMMSON或/和CARF预计将是一个新的治疗黑色素瘤的试剂。
推荐内容
-
运动蛋白在我们所有的细胞中跳舞
运动蛋白驱动我们细胞中的许多基本过程。正如ErikSchäffer教授和他的团队在一项新研究中所展示的那样,他们以跳舞动作移动。为了观察
-
怎么当心理医生治疗病人?
生活中,不管我们在跟自己独处还是跟别人相处的过程中其实我们会发现心理对一个人的影响是很大的。因此当我们发现自己有心理疾病的倾向...
-
浙江昨日新增本土确诊病例13例,新增本土无症状感染者19例
浙江昨日新增本土确诊病例13例,新增本土无症状感染者19例 4月24日024时,11个市报告新增确诊病例14例。其中境外输入病例1例(之前境
-
咸鱼已经被证明是导致鼻咽癌的食物之一
核心提示:说起鼻咽癌可能北方地区的人们比较陌生,因为患这种疾病的人群主要集中在广东、广西、湖南、江西和福建等地区。霉变咸鱼不仅...
-
近日一大姐骑单车突遭野猪围堵 随后野猪的一番举动让人哭笑不得
物种泛滥是一件让人们非常头疼的事情,虽然野猪在我们国家并不算常见,但还是会有特殊的情况发生。这不,近日就有一女子骑单车时突然遭到野
-
双相情感障碍小鼠模型中昼夜节律基因的红外振荡
情绪和情绪相关行为变化的分子基础尚不清楚。日本的研究人员通过研究双相障碍小鼠模型中大脑中的基因表达模式,成功地预测了类似情绪变...





