基因编辑的新形式减慢了小鼠的ALS进程
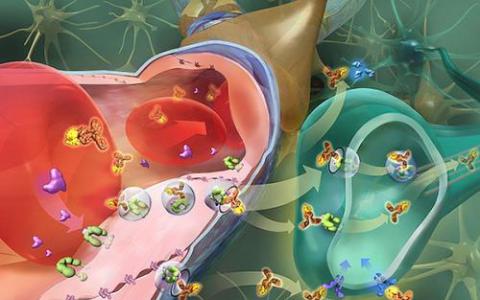
伊利诺伊大学香槟分校的科学家通过一种新的CRISPR基因编辑方法,使导致肌萎缩性侧索硬化症遗传形式的一种基因失活-一种无法治愈的衰弱和致命的神经系统疾病。这种新颖的治疗方法可缓解具有侵略性ALS的小鼠的疾病进展,改善肌肉功能并延长其寿命。
生物工程学教授托马斯·加伊(Thomas Gaj)与生物工程学教授巴勃罗·佩雷斯(Pablo Perez)共同领导了这项研究,他说:“不幸的是,ALS几乎没有治疗选择。这是重要的第一步,表明这种新形式的基因编辑可用于潜在地治疗疾病。”皮涅拉
该方法依赖于一种新兴的基因编辑技术,即CRISPR基本编辑器。
传统的CRISPR基因编辑技术会切割DNA分子的两条链,这会在DNA序列中引入各种错误,从而限制了其效率,并有可能导致基因组中许多意外突变。Perez-Pinera说,伊利诺伊州研究小组使用碱基编辑“将DNA序列的一个字母更改为另一个字母,而无需切断两条DNA链”。
盖伊说:“基础编辑器太大,无法与最有前途和成功的基因治疗载体之一-腺相关病毒一起传递到细胞中。” 但是,在2019年,Perez-Pinera的小组开发了一种将碱基编辑器蛋白分成两半的方法,该方法可以由两个单独的AAV颗粒递送。一旦进入细胞内,两半便重新组装成全长碱基编辑蛋白。
通过结合AAV基因传递和分裂碱基编辑器的功能,Gaj和Perez-Pinera靶向并永久禁用了突变的SOD1基因,该基因约占遗传基因ALS的20%。他们的研究结果发表在《分子疗法》杂志上。
许多ALS研究都集中于预防或延缓疾病的发作。但是,在现实世界中,大多数症状直到症状恶化才被诊断出来。进展缓慢而不是阻止进展可能会对患者产生更大的影响。”
研究人员首先在人体细胞中测试了SOD1碱基编辑器,以验证分裂的CRISPR碱基编辑器的重组和SOD1基因的失活。然后他们将编码基础编辑器的AAV颗粒注入携带突变SOD1基因的小鼠的脊柱中,该SOD1基因引起特别严重的ALS形式,该ALS在出生后几个月内使小鼠瘫痪。
该疾病在接受治疗的小鼠中进展较慢,具有改善的运动功能,更大的肌肉力量和更少的体重减轻。研究人员观察到,从疾病晚期到末期之间的时间增加了85%,并且增加了总生存期。
加平斯克说:“我们很高兴发现许多改善措施在疾病发作后就发生了。这告诉我们,我们正在减缓疾病的进展。”
基本编辑器在SOD1基因的起始位置附近引入了一个停止信号,因此,无论患者具有哪种基因突变,它都具有阻止细胞产生故障蛋白的优势。但是,它可能破坏基因的健康版本,因此研究人员正在探索靶向基因突变体拷贝的方法。
Gaj说:“展望未来,我们正在考虑如何将这项技术和其他基因编辑技术带入临床,以便有朝一日能够治疗患者的ALS。” “为此,我们必须开发能够靶向该疾病所涉及的所有细胞的新策略。我们还必须在其他临床相关模型中进一步评估这种方法的效率和安全性。”
Perez-Pinera说,基于碱基的编辑方法也具有利用遗传学方法治疗其他疾病的潜力。尽管ALS是该工具的首个演示,但他的小组正在进行研究以将其应用于Duchenne肌营养不良症和脊髓性肌萎缩症。
推荐内容
-
可视化穿过血脑屏障的寄生虫
据估计,世界上30%的人口长期感染寄生虫弓形虫(Toxoplasma gondii)。大多数人的感染都没有明显的影响,但对于免疫系统受到抑制的人,例如
-
ACROBiosystems与ProMab Biotechnologies合作开发免疫治疗产品
重组蛋白的领先制造商ACROBiosystems宣布,他们已与ProMab Biotechnologies签署合作协议,ProMab Biotechnologies是单克隆抗体和CAR-T细
-
基因匹配可以帮助科学但会引发隐私问题
一个人能从13个小小的DNA片段中真正弄清楚多少人?乍一看,并不多 - 在遗传学领域,13是微不足道的。但是一项新的研究表明,可能足以推断
-
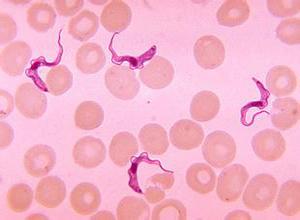
发现一种潜在的治疗靶点来对抗锥虫
Yaser Hashem在CNRS的实验室建筑和研究中心的团队发现了一种新的潜在治疗靶点 - 位于核糖体中 - 用于对抗锥虫寄生虫。使用低温电子显
-
自恐龙时代以来 珊瑚和微藻一直在一起
根据一个国际科学家小组的最新研究,珊瑚礁生态系统中心的珊瑚藻共生远比怀疑的要长,并且经历了地球气候的重大变化。该团队由宾夕法尼...
-
研究人员将基因活动与小型雄鱼直接联系在一起
称之为本能,但有些东西迫使某些动物以某种方式行事,也许是基因中的程序。研究人员将基因活动与本能行为直接联系在一起的小型雄鱼中,...
-
研究人员在新的小鼠模型中缓解了精神分裂症的症状
尽管进行了广泛的研究工作,精神分裂症仍然是最不了解的脑部疾病之一。一个有希望的研究领域是脑细胞表面的受体,有助于感知生长因子。...
-
微小的DNA读取器以促进抗癌药物的发展
DNA很小。真的,真的,小。因此,当研究人员想要研究单链DNA的结构时,他们不能只是拔出他们的显微镜:他们必须要有创造力。在本周发表在
-
新版人类蛋白质图谱
今天,推出了第15版人类蛋白质图谱。新版本包括来自不同来源的数据,这使得可以对RNA和蛋白质水平的组织谱进行比较。仔细观察人体组织或细
-
科学家对加利福尼亚双斑八爪鱼的基因组进行序列分析
来自日本和美国的一个国际遗传研究小组对加利福尼亚常见的双斑章鱼(Octopus bimaculoides)的基因组进行了测序和分析,使其成为有史以来第