研究描绘了结核病早期进展的遗传学
虽然感染结核菌的18亿人中绝大多数人从未患过活动性疾病,但估计有5%至15%的人确实患有全面感染 - 其中大约一半是在接触后的18个月内。
为什么有些人在感染后很快就会患上明显的疾病,而其他人几十年来一直感染无声感染并且显然仍然健康?

这个问题一直困扰着微生物学家,传染病专家和公共卫生专家,他们在抗击结核病方面处于领先地位,这种疾病在全球范围内的生命比任何其他传染性病原体都要多。
现在,来自哈佛医学院,布莱根妇女医院,麻省理工学院和哈佛大学,秘鲁Socios en Salud和其他机构的科学家们的研究提供了一个答案:早期疾病进展的一些风险是由几种基因变异驱动的。 ,其中至少有一个控制着关键的免疫功能。
该研究于8月21日在Nature Communications上发表,被认为是第一项大规模研究,旨在探索生活在同一家庭中的早期结核病进展的遗传基础,并确认有活动性和潜伏性感染。研究小组表示,这是研究的一个特殊优势,因为它确保了有意义和直接的比较,使科学家能够区分受感染的进展者和受感染的非进展者。
研究人员补充说,可以肯定的是,这不是整个故事,更多的基因可能会被发现作为早期疾病进展的驱动因素。他们说,这些基因很可能分布在基因组的许多区域,就像其他疾病一样,例如心血管疾病或糖尿病 - 多因素疾病,这些疾病是由多种基因突变引起的,并受环境和生活方式因素的影响。
在细菌感染后不久,早期进展为活动性结核病在生理上不同于迟发性疾病,其在休眠数年或数十年后发展,通常是由于衰老或免疫抑制。
长期以来,科学家一直怀疑免疫系统因素推动了从潜伏性结核感染到明显疾病的进展,假设那些免疫系统在感染后很快就无法迅速进入明显疾病的人。
这项涉及秘鲁利马感染结核病的人的研究确定了干扰免疫控制并导致早期进展的精确遗传区域。通过这项研究,该研究证实了基因介导的免疫在结核感染后疾病发展中的作用。此外,该研究指出早期与晚期结核病的不同遗传基础,强调了这两种疾病形式的根本不同。
“我们研究的目的是描述感染后不久发展为结核病的人与不发展为明显疾病的人之间的遗传差异,”全球卫生部教授,联合高级调查员Megan Murray说。哈佛医学院Blavatnik研究所的社会医学。“我们的结果表明,早期结核病进展是一种高度遗传性状,并且在多年休眠后遗传上与结核病再激活不同。”
哈佛医学院医学教授,布莱根妇女医院临床医师Soumya Raychaudhuri说,了解早期疾病进展背后的遗传机制可以为制定干预措施提供信息,例如疫苗或药物可以防止人们感染后发病。广泛研究所的成员。
此外,Raychaudhuri补充说,这些研究结果可能会导致设计可以帮助临床医生确定谁有早期进展风险的测试。
研究人员首先检查了秘鲁人公开提供的全基因组数据集。他们归巢于DNA的微小区域,称为单核苷酸多态性或SNP(发音为“snips”)。每个SNP代表基因组字母表中单个核苷酸或单个字母的差异。SNP可以改变基因的功能,以及发现它们的调控序列。为了提高分析的准确性,研究人员确定了秘鲁人群特有的SNP,调整了他们的基因分型测试,以反映这种特定种群的变异。
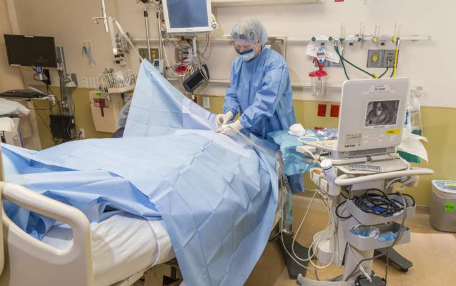
接下来,研究人员从2000多名患有活动性结核感染的人和2000名住在同一家庭的人中获得了DNA样本,这些家庭也感染了结核病但没有活动性疾病。为了确认明显无病的室友确实感染了结核病,研究人员使用标准的结核病皮肤测试,血液测试和肺部X射线成像对他们进行筛查,以检查体内是否存在结核病。研究人员在2个月,6个月和12个月时重复这些测试。这种方法使科学家能够比较共享相同环境并具有相同或非常相似的疾病暴露的个体之间的遗传风险。
该分析追踪了对3号染色体区域易感性的影响,该区域涉及调节ATP1B3的表达,ATP1B3是一种已知影响免疫细胞功能的蛋白质,称为单核细胞,其在先天免疫中具有关键功能,包括检测病毒和细菌的存在。入侵者检测和破坏有缺陷或受感染的细胞。
研究人员假设基因变异干扰调节单核细胞功能的蛋白质的表达,干扰免疫细胞执行关键功能的能力,从而增加早期结核病进展的风险。
有人提出与人类白细胞抗原复合物区域中基因组的其他区域早期进展的关联,其编码作为免疫系统关键部分的蛋白质。该复合物涉及区分人类蛋白质和外来入侵者如细菌和病毒。
“我们发现的风险区域可能在结核病进展的免疫反应中起着至关重要的作用,但它们可能不是故事的结尾,”主要作者杨洛说,他是哈佛医学院的医学研究科学家和讲师。布莱根妇女队。
罗补充说,随着遗传样本的大小和相关研究的不断增加,可能会发现更多的DNA区域导致早期疾病进展的易感性。
“可能还有许多其他等位基因在基因组周围传播的效果较弱,”Raychaudhuri说。相比之下,遗传变异似乎占克罗恩病病例的28%。研究人员表示,全基因组关联研究已经确定了大约200个等位基因,这些等位基因导致了克罗恩病遗传风险的这种变异。
研究小组表示,感染,特别是慢性传染病,在非常不同的阶段发挥作用,新的研究确定了其中一个阶段背后的一些遗传因素。
“我们相信我们的分析是长途旅行的第一步,”Raychaudhuri说。“寻找干预这些不同阶段的新方法,制定可优化宿主免疫力或干扰病原体适应性的策略。”
推荐内容
-
新研究发现吸烟和肥胖的ARDS患者生活质量较差
一项对曾经致命的急性呼吸窘迫综合症(ARDS)存活的患者进行的新研究发现,他们随后的生活质量与生活方式因素更多地相关,而不是与他们在医院
-
自恐龙时代以来 珊瑚和微藻一直在一起
根据一个国际科学家小组的最新研究,珊瑚礁生态系统中心的珊瑚藻共生远比怀疑的要长,并且经历了地球气候的重大变化。该团队由宾夕法尼...
-
守护解放西是真人真事吗为什么叫守护解放西?守护解放西3小玲孩子
【导读】你知道守护解放西第三季吗?据消息显示,《守护解放西第三季》是哔哩哔哩、中广天择联合出品的警务纪实观察类真人秀。该节目通过观
-
当它“裸露”时新发现的小RNA片段可以保护基因组
我们的基因组是雷区,带有潜在破坏性的DNA序列,成千上万的哨兵守卫着这些序列。这些称为表观遗传标记的哨兵在这些斑点处附着于双螺旋,并
-
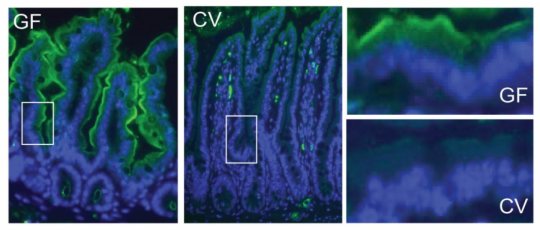
肠道微生物组调节肠道免疫系统
科学家早就知道,肠道内的细菌,也称为微生物组,可以为宿主提供各种有用的功能,例如在消化过程中分解膳食纤维,制造维生素K和B7。然而,
-
非编码DNA的重复可能影响人类特异性状的进化
根据美国佛罗里达州奥兰多举行的美国人类遗传学会(ASHG)2017年会议上提出的结果,人类基因组中大部分非编码DNA的复制可能导致人类与非人类
-
【悲剧】女子大雪天翻墙回家被卡一整晚 第二日路人目睹了恐怖一幕
【摘要】最近,俄罗斯被冻死悲剧频频发生,那么,真相究竟是什么呢?据最新消息显示,此前,12月4日,一名三岁女孩半夜梦游到家门口时也被冻
-
CRISPR编辑的水稻植物产量大大提高
普渡大学和中国科学院的科学家团队利用CRISPR Cas9基因编辑技术开发了多种水稻,这些水稻的谷物产量增加了25-31%,而且几乎不可能通过
-
科学家对两种大黄蜂物种的基因组进行测序
遗传研究人员已经对两种主要的大黄蜂物种进行了测序和分析,它们是欧洲长尾大黄蜂(Bombus terrestris)和北美常见的东部大黄蜂(Bombus imp
-
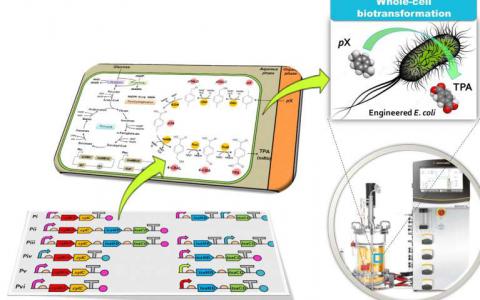
通过工程化大肠杆菌将生物基对二甲苯氧化成对苯二甲酸
KAIST研究人员建立了一种高效的生物催化系统,用对二甲苯(pX)生产对苯二甲酸(TPA)。它将使这种工业上重要的大宗化学品以更环保的方式提供。