研究检查了候选埃博拉疫苗的安全性和免疫反应
在2016年4月19日出版的《美国医学会杂志》上发表的一项研究中,英国牛津大学FRCPCH医学博士Matthew D. Snape和其同事进行了一项1期试验,以评估两种候选埃博拉疫苗的耐受性和免疫原性,26型腺病毒载体疫苗(Ad26.ZEBOV)和改良的安卡拉载体疫苗(MVA-BN-Filo)。
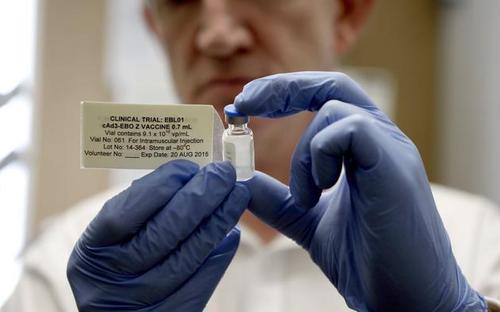
自2013年12月在几内亚发现首例病例以来,西非最近爆发的埃博拉病毒病已造成28,600多例病例,并有11,300例死亡。国际上的回应包括加速了几种候选埃博拉疫苗的临床开发。在非人类的灵长类动物中,用Ad26载体接种的疫苗能够产生高达75%的抗埃博拉病毒攻击的保护作用。
对于本研究,参与者(18-50岁的健康志愿者)被随机分为4组,在这些组中,他们同时按5:1的比例随机接受研究疫苗或安慰剂。接受活性疫苗的患者先接种Ad26.ZEBOV或MVA-BN-Filo,然后在28天或56天后使用替代疫苗加强免疫。第五天,开放标签组在14天后接受了MVA-BN-Filo增强的Ad26.ZEBOV。该试验在英国牛津进行
在87名研究参与者中,有72名被随机分为4组,每组18名,开放标签组包括15名。四名参与者未接受加强剂量;在75个月的研究中,对75名研究疫苗接受者中的67名进行了随访。用Ad26.ZEBOV初次免疫后观察到免疫反应。MVA-BN-Filo加强免疫后,特异性免疫力持续提高。用Ad26.ZEBOV或MVA-BN-Filo免疫未导致任何疫苗相关的严重不良事件。
“我们的数据显示,与MVA-BN-Filo相比,Ad26.ZEBOV初免产生了初始的免疫反应,并且有证据表明在非人灵长类动物模型中单独给予这种疫苗是有保护的。因此,预计该初次剂量可产生至少部分抗埃博拉病毒的保护;因此,目前正在第1、2和3期研究中进一步评估带有MVA-BN-Filo增强作用的Ad26.ZEBOV首要时间表。”
推荐内容
-
怀孕期间住院的女性肾脏损伤率上升
最近的一项分析显示,怀孕期间住院的妇女,尤其是患有糖尿病的妇女,其急性肾损伤的发生率增加。另外,与妊娠相关的急性肾损伤的妇女在...
-
12.8南京市鼓楼区封控区隔离区疫情消息公布 今日,鼓楼区南
南京一社区发现酸检阳性者!涉及居民实施封控管理。据消息显示,12月8日,南京市鼓楼区南秀村社区报告出现一例新冠肺炎病毒核酸检测阳性人员
-
11月26日上海疫情最新数据公布 昨日,上海市新增3例本土病例
想必大家都知道,上海,简称沪或申,是中华人民共和国省级行政区、直辖市、国家中心城市、超大城市。那么,你知道上海目前疫情什么情况...
-
科学家绘制了当今人类的尼安德特人 德尼索瓦先祖的地图
哈佛医学院的David Reich博士及其同事绘制了Denisovan和尼安德特人血统的世界地图,涵盖了120个不同的人群。他们的分析表明,Denisovan与
-
史前美洲人中复杂的远古DNA 以环境为基的变化
现在的科学家对来自久远时间的DNA进行综合研究时,发现一些很复杂的结果。曾经人类在美洲定居的情况是非常复杂的,这都是通过测试基因得出
-
科学家们开发了一个稳定的平台 将瘢痕组织重新编程为健康的心脏
每年有790,000名美国人心脏病发作,这会使心脏受损的疤痕组织受限,并限制其有效击败的能力。但是,如果科学家能够将称为成纤维细胞的瘢痕
-
高脂饮食不仅影响您的外表 还影响您的大脑
许多研究指出了不健康的饮食与肥胖之间的关系,但并未探讨饮食如何导致大脑的神经系统变化。耶鲁大学最近的一项研究发现,高脂饮食会导...
-
华大基因董事长汪建一行来访交流
在基因领域,绕不开的是拥有一系列头衔的汪建,他不仅仅是华大基因董事长,也是深圳华大基因研究名誉院长。在11月28日下午,汪建带一行专业
-
尼安德特人衍生的DNA对现代人的性状有重要影响
由范德比尔特大学遗传学家约翰·卡普拉(John Capra)领导的一大批科学家发现,尼安德特人(Neanderthal)衍生的DNA与人类疾病之间的惊人关联
-
婆媳关系心理医生咨询案例
在心理咨询中遇到过很多是婆媳关系问题的家庭,终结了一些修复婆媳关系的方法如下:婆媳关系不好相处、你会发现只要你在婆婆堆里,定有...