实验疫苗产生的抗体可以中和多种艾滋病毒株
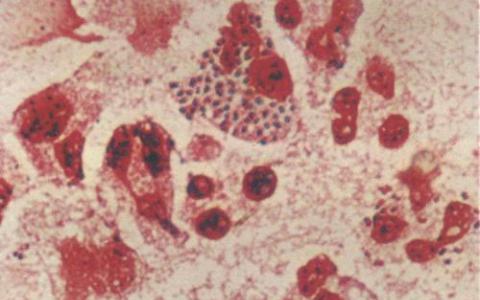
由斯克里普斯研究中心和非营利性疫苗研究组织IAVI的科学家开发的一种实验性艾滋病毒疫苗已经达到了一个重要的里程碑,它可以产生抗体,中和多种艾滋病毒毒株。

在兔子身上进行的试验表明,这些“广泛中和”的抗体(bnab)至少针对病毒的两个关键部位。研究人员普遍认为,如果要对这种不断变化的病毒提供强有力的保护,疫苗必须诱导bnab进入艾滋病毒的多个位点。
这一发表在《免疫》(Immunity)杂志上的有希望的结果表明,研究人员距离开发有效的艾滋病毒疫苗又近了一步——自1983年发现艾滋病毒以来,这一直是医学科学的一个主要目标。
这是原则的初步证明,但也是重要的,我们现在正在努力优化这种疫苗设计。”
理查德·怀亚特博士,该研究的资深作者,斯克里普斯研究所免疫学和微生物学系教授
据联合国艾滋病规划署称,全球约有3500万人死于由艾滋病病毒感染引起的免疫缺陷综合症。目前约有3800万人感染了艾滋病毒。抗病毒药物可以使感染艾滋病病毒的人存活下来,并降低他们将病毒传染给他人的能力,但这些药物不能清除感染,必须无限期服用。研究人员早就认识到,需要一种预防疫苗来消除作为主要公共卫生威胁的艾滋病毒,这种疫苗对未受感染的人来说成本较低。
艾滋病毒的快速突变率和其他逃避免疫攻击的机制使它成为疫苗设计者极为困难的目标。但是,怀亚特和他的团队进行的测试证实,疫苗接种可以诱发所需的抗体,从而提供广泛的艾滋病毒保护。这些被疫苗专家称为bnab的抗体可以中和多种HIV毒株,因为它们与病毒的关键位点相结合,而这些位点在不同毒株之间变化不大。感染艾滋病毒的人有时会产生bnab作为抗体反应的一部分,但很少发生,通常是在感染很长时间之后。艾滋病毒疫苗设计者面临的主要挑战是找到刺激免疫系统(大多数或所有个体)的方法,使其产生能攻击病毒多个易损位点的bnab,从而抵御高比例的艾滋病毒毒株。
怀亚特及其同事设计的疫苗的核心是一种基于艾滋病毒“Env”蛋白的病毒模拟蛋白。正常情况下,多个布什样Env蛋白拷贝散布在每个球形HIV颗粒的表面。每种Env蛋白都包含一种分子机制,使其能够与免疫细胞上称为CD4的受体结合,并利用该受体作为进入细胞的门户。研究人员设计了Env的一个版本,该版本模拟真实的Env的基本结构,同时又足够稳定,可以用作疫苗。为了以一种类似于真正的HIV病毒颗粒的方式来呈现它,他们创造了病毒大小的合成脂肪相关分子的球体,即“脂质体”,这些脂质体密集地散布着经过设计的Env蛋白质。
在一种天然的HIV环境蛋白上,被称为聚糖的与糖相关的分子丛通常帮助保护所有重要的CD4结合位点免受免疫攻击。作为一种初始的“启动”免疫,研究人员使用了Env的版本,其中CD4结合位点周围的这个聚糖盾被部分移除。
怀亚特说:“我们的想法是更好地暴露这个部位,从而在一开始就激发广泛的抗体反应。”
随后48周的增强免疫使用带有修复的聚糖的Env蛋白,来选择针对CD4结合位点的抗体,但也可以通过这个屏障。加强注射中的Env蛋白也是根据不同的艾滋病毒毒株混合使用的,以促进对Env结构的抗体应答,而这些结构在这些毒株之间没有变化。
研究小组按照他们的疫苗接种策略为12只兔子接种了疫苗,并将结果与只接受单一的、多糖屏蔽版Env的对照组进行了比较。他们发现他们的疫苗策略有一个更好的反应,5只兔子产生抗体,可以中和多个HIV分离物。
研究人员分析了反应最强烈的兔子的抗体,并确定了两种不同类型的bnAb。其中一种被他们称为E70的抗体以一种不同寻常的方式阻断了CD4的结合位点,部分方式是抓住其中一个屏蔽聚糖。另一个是1C2,它击中了Env上一个不同但众所周知的易损点,即复杂蛋白质的两个关键片段之间的接口。抗体1C2的结合显然破坏了Env的稳定性,使其不再能够介导HIV进入宿主细胞。这种抗体的中和宽度也不同寻常,在208个不同的艾滋病毒分离株中,有87%被阻断。
怀亚特说,这一发现是一个重要的证明,表明如果采用正确的方法接种艾滋病毒疫苗,可以实现将bnab诱导到病毒的多个位点的目标。
这组科学家正继续在小动物模型上测试和改进他们的疫苗策略,并希望最终在猴子和人类身上进行测试。
推荐内容
-
研究探讨了病原体如何影响鸟类迁徙
长距离动物迁移是否促进或阻碍病原体传播取决于感染如何影响迁移宿主的途径和时间。在动物学杂志的一项研究中,研究人员发现,通常感染...
-
研究发现物理力会影响细菌的毒素抵抗力
两位康奈尔大学研究人员在一个孩子的生日聚会上进行了随机交谈,这导致了人们对细菌如何抵抗毒素的协作和新的理解,这可能会为抗击有害...
-
如何让孩子理解道歉的意义?
当孩子们说对不起时,他们是在吸取教训还是只是在重复空话?你有没有觉得应该道歉,并在没有得到道歉时感到沮丧?你有没有发现很难表达...
-
科普男性滴酒不沾对身体好吗及飲食街油煙滾滾局長怎麼看
男性滴酒不沾对身体好吗?中国老百姓喜好饮酒,这是世界公认的,咱们的白酒度数很高,虽然在这样的冬天喝了可以暖身,但是经常酗酒就会严重
-
信贷科技和财富管理科技两翼齐飞 宜人金科持续赋能行业
宜人金科旗下宜信普惠作为的信贷科技板块,致力于利用移动互联网、大数据、人工智能等为小微企业主、农户、工薪阶层等中国高成长性人群...
-
公共水稻基因组资源对育种者来说是有利的
康奈尔大学领导的国际研究团队推出了一套开放获取的基因组资源,这将极大地加速遗传学家和育种者将基因与水稻重要性状联系起来的能力。...
-
研究产生E组抗体的细胞有助于对抗过敏
Sechenov大学的研究人员和他们来自俄罗斯和奥地利的同事总结了关于细胞产生E组抗体的所有已知信息。这些分子是大多数过敏反应的原因,包...
-
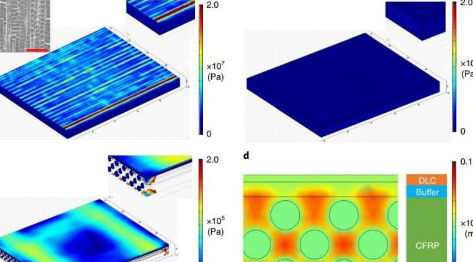
复合材料的新型纳米屏障可增强航天器的有效载荷
萨里大学已经为超轻量和稳定的碳纤维增强聚合物(CFRP)开发了一种坚固的多层纳米屏障,可用于构建未来太空任务的高精度仪器结构。CFRP用于当
-
身体的每个器官都有一定程度的自我修复能力
受伤后,身体的每个器官都有一定程度的自我修复能力。作为此过程的一部分,疤痕组织会形成,然后在愈合完成后退去为正常组织腾出空间。...
-
激发病毒屏蔽上的振动并对其造成伤害的技术 因此它不再具有功能
是否有可能在受感染的组织上发光,只杀死病毒,保持健康组织完好无损?一个父子团队将物理学和生物学相结合,以证明它确实是可能的。亚利桑