最新的FDA认证前工作模式获得了不高的支持
在周一发表的评论中,FDA关于其软件预认证计划的愿景的第三次迭代获得了行业组织AdvaMed和医学影像与技术联盟的坚定支持。法定权力的问题仍然迫在眉睫,AdvaMed认为该计划的承诺“未经立法授权可能无法完全实现。”
在 美国医学协会提出在其评论担心,某些人工智能和机器学习产品带来独特的风险和不应该被允许进入该程序,直到进一步的更改。
FDA表示,按照目前的法定授权,它仍有望在今年正式启动“预认证”试验计划。

Pre-Cert计划旨在通过预先筛选精选的公司来进行软件开发并将其作为医疗设备打补丁,从而使公司更容易将其推向市场,而无需进行机构审查。
最新的工作模式,在一月份发布,概述了FDA的计划使用在试点阶段,与流线型的审查演唱会从头途径 ,其中 该机构 希望评估是否预先清关公司相当于一个传统的营销提交。
包括专员斯科特·戈特利布(Scott Gottlieb)在内的该机构官员表示,该机构仍计划在2019年对该试点计划进行测试。包括Fitbit,Pear Therapeutics和Apple在内的9家公司都参与其中。
AdvaMed在其评论中列出了其希望在计划最终完成之前要进行的调整的清单,其中包括基于风险的方法来评估预结算公司的关键绩效指标“以保持卓越的一致性水平”,以适应国际医疗器械监管者论坛针对美国市场的风险分类框架,并在FDA收到确认文件时建立了为期五天的审核时间表。
设备游说团体还重复要求FDA对医疗设备中的软件(不仅是作为医疗设备的软件)开放Pre-Cert。
AdvaMed成员GE Healthcare认为,在没有国会采取行动的情况下,不得将510(k)的某些SaMD豁免于该计划的“无审查”途径。
“在工作模型的最新版本中,尚不清楚可信赖的经过预认证的组织是否有能力以比今天的监管模型所允许的速度更快地将软件医疗设备投放市场”,GE Healthcare数字事务监管总监Camille Vidal写道。健康。
软件公司律师布拉德·汤普森(Brad Thompson)在一次采访中对MedTech Dive表示,尽管他没有向会议记录表提交新的评论,但他仍然对该程序在最新工作模式下对小型公司的效用表示担忧。
汤普森说:“我认为,不幸的是,眼下,这家公司已经被一些大型的老牌公司所采用,而且该计划确实对初创企业没有帮助。” “这很遗憾,因为初创公司是众多创新的源泉。我很乐意看到Pre-Cert Program进行了修改,以使其对这些创业公司更具吸引力。”
同时,AMA的反馈表明,如果FDA为较小的公司提供更多的宽大处理,则医生可能不信任通过快速途径清除的产品。
AMA表示:“我们重申先前对[Pre-Cert Program]要素的担忧,这将破坏FDA推广[Pre-Cert Program]作为卓越模型的努力,并侵蚀医生的信任,认为通过此途径开发的产品是安全有效的,”首席执行官詹姆斯·马达拉(James Madara)写道。
国会中的一些民主党人也表示担心该机构正在采取过于宽容的态度,从而损害安全。
推荐内容
-
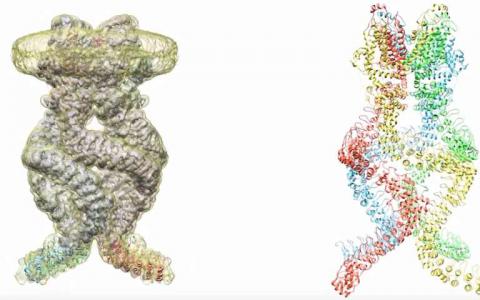
单细胞古菌如何确定游泳的方向
Tessa Quax博士已经确定了古细菌用于确定游泳方向的中心蛋白质的结构。古细菌是没有细胞核的单细胞生命形式。她还研究了从古生物环境到其
-
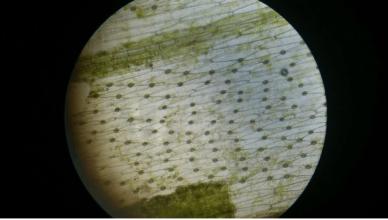
两个植物细胞“热点”告诉细胞在哪里输入其资源
Brandizzi实验室的科学家们正在增加我们对扩大iconendocytosis的理解,植物细胞如何从周围环境中输入分子。在胞吞作用期间,细胞识别外部分
-
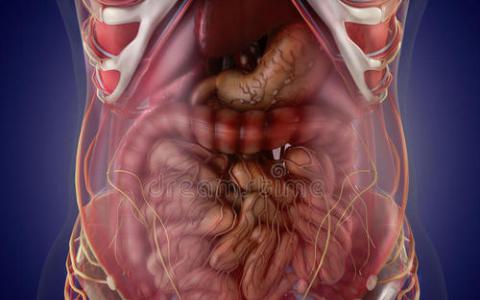
研究清除了增长替代身体器官的方法
一项涉及蒙纳士大学科学家的发现有望为使用患者自身干细胞生产受损心脏,肾脏和肠道的替代器官铺平道路。该研究由蒙纳士大学澳大利亚再...
-
分子弹簧产生苍蝇的触觉和听觉感
随着感官的去,没有什么比我们的触觉更直接和具体。因此,令人惊讶的是,在分子水平上,我们的触觉仍然知之甚少。我们的每一种感官都依...
-
尿液中的抗抑郁药使鱼类不再害怕掠食者
抗抑郁药正在进入我们的湖泊和河流 - 他们正在制造淡水鱼,而不是被捕食者盯着。蒙纳士大学博士候选人杰克·马丁(Jake Martin)研究了东
-
研究证实人工智能系统在前列腺癌诊断中的准确性
《柳叶刀肿瘤学》今天发表了一项研究结果,证明人工智能(AI)系统在组织样本中诊断前列腺癌的准确性。 这项由瑞典卡罗林斯卡研究所(Ka...
-
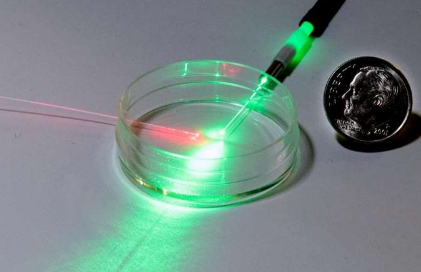
用光追踪实验室生长的组织
有一天,医生希望为在战斗中失去手臂的士兵,需要新的心脏或肝脏的孩子以及许多其他有紧急需求的人种植四肢和其他身体组织。如今,医疗...
-
索非布韦的研发历程
丙型肝炎(简称丙肝)是由丙型肝炎病毒(HCV)感染引起的病毒性肝炎,全球有超过1 5亿人口感染HCV,我国也有1000万人感染丙肝。该病隐匿性强,
-
Merck KGaA将扩大瑞士Aubonne制造基地
德国达姆施塔特的Merck KGaA今天表示将在瑞士Aubonne进行1 5亿欧元(1 68亿美元)的生物制剂生产基地扩建,旨在通过提高生产能力来满足日益
-
失败的癌症药物看起来有希望硬皮病和其他纤维化病症
十六年前,梅奥医学院的一个研究小组发表的研究结果表明,一种名为TRAIL的蛋白可以杀死导致肝纤维化的细胞,但似乎没有人跟进这些发现。现