FDA敦促供应商 制造商使用一次性部件过渡到十二指肠镜
该机构表示,虽然美国食品和药物管理局正在建议过渡,但立即移除传统设备可能导致设备短缺并阻止患者接受重症监护。
美国食品和药物管理局每年进行超过50万次内镜逆行胰胆管造影术,明确了使用固定端盖十二指肠镜的现有手术应该继续进行,因为“因为目前传统的固定端盖十二指肠镜完全撤出市场是不可行的。”

“我们认识到,从传统的十二指肠镜到创新模式的全面过渡需要时间,并且由于成本和市场可用性,所有医疗机构不可能立即过渡,”CDRH主任Jeff Shuren在一份声明中说。“我们将继续与制造商合作,增加一次性帽十二指肠镜的供应,并开发其他新的和创新的设备设计,以进一步减少或消除患者感染的风险。”
该机构还宣布将于2019年底召开一个咨询委员会,讨论十二指肠镜污染率,后处理方法和新的十二指肠镜设计。FDA还要求制造商在市场上已有的固定端盖十二指肠镜标签上加入实际污染率。
迄今为止,FDA已经从Fujifilm和Pentax清除了两个一次性端盖十二指肠镜,该机构表示,与传统的固定端盖装置相比,可以将患者与患者之间的污染风险降低一半。
周四,FDA宣布它正在订购新的上市后监督研究,以“验证新设计降低污染率。”一旦完成,该机构表示,预计一次性包装十二指肠镜上的标签将更新,以包括污染率数据,以帮助患者和提供者做出医疗决定。
Fujifilm于3月28日获得其一次性远端帽模型的许可,他告诉MedTech Dive,它“正在最终确定该设备的分销计划”。
奥林巴斯目前正在开发一种一次性端盖十二指肠镜,并计划“尽快”申请FDA批准,据公司发言人称。
奥林巴斯发言人在一封电子邮件中告诉MedTech Dive,“我们正在与FDA合作,并支持他们建议逐步过渡到使用一次性部件的十二指肠镜。” 该公司在市场上维持其十二指肠镜仍然可以安全使用,并指出FDA的安全通信状态感染风险仍然“相对较低”。
Olympus和Fujiflm设备的人为因素研究发现,当前的用户指导材料不足以确保用户坚持核心后处理领域,如预清洗,手动清洗和手动高级消毒。Pentax的初步研究符合验收标准,但在这三个方面存在一些“知识和表现上的失败或接近失误”。
据该机构称,这些公司正在与FDA合作修改后处理手册并进行额外的测试。
开发一次性十二指肠镜的公司Ambu的医学主任Stephen Spanos告诉MedTech Dive,FDA呼吁过渡到具有创新设计的示波器,以促进或消除对后处理的需求,这对其商业模式来说是一个“大好机会”。
斯潘诺斯说:“从临床角度和公共卫生角度来看,患者仍然利用现有技术仍然具有超级关键性,因为目前不做这些手术的风险远大于感染风险。” “直观的是,单一使用,不仅仅是来自Ambu,肯定会属于这个指导方针,绝对可能是一个重要的参与者。”
波士顿科学公司也希望通过一次性十二指肠镜进入市场。在2018年6月的投资者网络广播中,波士顿科学公司内窥镜检查高级副总裁Art Butcher表示,这种设备代表了超过10亿美元的市场机会,并有可能减少后处理问题,提高成本效益并最大限度地减少资本投资。
推荐内容
-
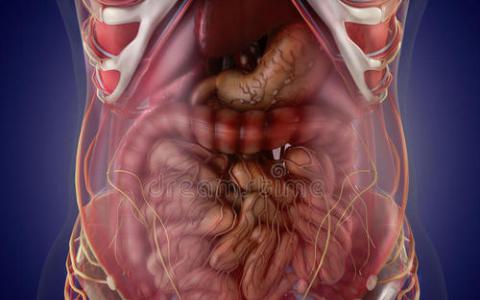
研究清除了增长替代身体器官的方法
一项涉及蒙纳士大学科学家的发现有望为使用患者自身干细胞生产受损心脏,肾脏和肠道的替代器官铺平道路。该研究由蒙纳士大学澳大利亚再...
-
保护木材的新工艺可能比压力处理更具优势
压力处理(包括将木材放入加压的水密罐中并迫使化学品进入板中)已经使用了一个多世纪,以帮助防止真菌在潮湿环境中造成木材腐烂。现在,...
-
研究人员开发可穿戴纸基紫外线传感器
由皇家墨尔本理工大学(RMIT University)领导的国际研究人员团队开发了基于纸张的紫外线传感器,该传感器可以帮助人们管理维生素吸收并避免
-
威胁巧克力的真菌放弃了有性生殖进行克隆
普渡大学的研究人员发现,一种对可可植物构成严重威胁的真菌病 - 巧克力来源 - 可以克隆地繁殖。真菌Moniliophthora roreri引起霜冻腐
-
这就是病毒如何使免疫系统失活导致癌症
这并不是病毒导致癌症的新消息。例如,人乳头瘤病毒(HPV)几乎导致全世界每年超过50万例宫颈癌病例。这是有道理的:通过驱动受感染细胞的增
-
SpatialOMx如何在疾病研究中提供新的见解
在接受Bruker Daltonics公司用途披露经理香农·科尼特博士(Shannon Cornett Ph D )的采访时,他讨论了MALDI的使用,并在对这种疾病...
-
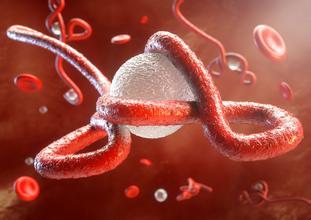
新研究缓解了对空中埃博拉病毒的担忧
去年秋天在埃博拉疫情的高峰期出现了一种令人恐惧的新可能性:一种可使该疾病在空中传播的突变。现在,佛罗里达大学的研究人员已使用来...
-
研究表明孕妇在透析方面的种族差异
由于生育能力受损,接受透析的妇女怀孕并不常见。辛辛那提大学(University of Cincinnati)的一项新研究发现,患有某些肾脏疾病的患者中,
-
新型纳米颗粒会侵蚀掉引起心脏病发作的部分斑块
密歇根州立大学和斯坦福大学的科学家们发明了一种纳米粒子,它从内部到外部侵蚀导致心脏病发作的斑块的一部分。 MSU生物医学工程副教授...
-
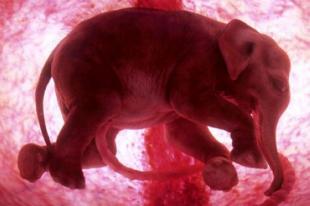
哺乳动物胚胎中20000个细胞的第一个'细胞图谱'
Wellcome-MRC剑桥干细胞研究所的科学家利用尖端技术分析了20,000多个细胞,制作了第一个描述哺乳动物胚胎发育早期所有主要细胞类型的细胞图