ER融合蛋白和膜转运
本周在PNAS上发表的一项研究中,中国科学院生物物理研究所的科学家研究了内质网(ER)的分泌途径。具体而言,他们发现ER融合蛋白atlastin(ATL)参与调节ER中的货物移动性和COPII形成。该发现提供了对管状ER网络的生理作用的重要见解。
在真核细胞中,ER形成连续片和小管的复杂网络。小管由一类完整的膜蛋白,网状结构和REEP形成,随后通过ATL以三向连接的形式连接。
哺乳动物细胞中ATL的缺失或突变导致长的,无支链的ER小管,表明小管之间缺乏融合,并且人ATL1的突变与遗传性痉挛性截瘫有关。该团队以前的工作表明,ATL及其同源物介导了ER的融合,特别是管状网络,但管状ER网络的特定生理功能仍不清楚。
进一步的研究发现,在没有ATL的情况下,ER的移动性较差。有趣的是,ATL R77A可以恢复货物的流动性和COPII形成,它能够束缚但不能融合ER小管。折叠和适当修饰后,货物蛋白通过COPII包被的囊泡离开ER。研究人员发现,在ATL缺失的细胞中,细胞周围的COPII形成急剧减少,ER输出变得有缺陷。虽然ER退出站点启动不受影响,但许多站点未能招募COPII亚基。随后,他们的体外囊泡释放测定显示,在缺乏ATL的细胞中,货物包装进入COPII囊泡的效率显着降低。
这些发现表明ATL介导的膜束缚在维持ER内容物的必要移动性中起关键作用,以允许将货物蛋白质有效包装成COPII囊泡。已经表明膜张力影响膜组分的移动性。ATL的活性,特别是在膜束缚中,可能有助于调节ER中的膜张力。
推荐内容
-
科学家展示了南加州近海微生物的进化原理
在南加州近海的海浪中,细菌战与生命本身一样古老。USC海洋生物学家在这里完成了一项全面的新研究,该研究表明细菌和病毒采用的策略相互竞
-
猪肠道中有超过700万个细菌基因
来自INRA(法国),哥本哈根大学和SEGES(丹麦),BGI-深圳(中国)和NIFES(挪威)的国际研究人员联合会现已建立了猪肠道中第一个细菌基因目录。该
-
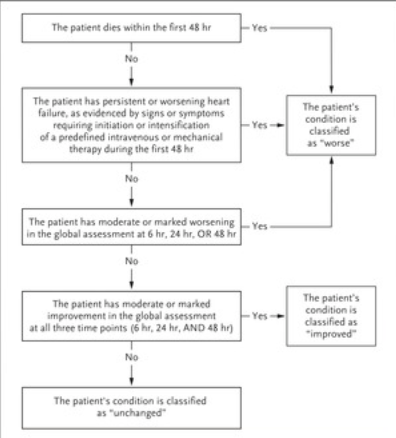
Evacetrapib和高危血管疾病的心血管结果
胆固醇酯转移蛋白抑制剂evacetrapib实质上提高了高密度脂蛋白(HDL)胆固醇水平,降低了低密度脂蛋白(LDL)胆固醇水平,并增强了细胞胆固醇的
-
研究产生E组抗体的细胞有助于对抗过敏
Sechenov大学的研究人员和他们来自俄罗斯和奥地利的同事总结了关于细胞产生E组抗体的所有已知信息。这些分子是大多数过敏反应的原因,包...
-
在博物馆中发现的新植物物种可能已经灭绝
在日本自然历史博物馆保存的单一非光合作用植物标本已被确定为新物种。然而,这种物种很可能已经灭绝。这些研究结果将于9月13日在Phytotaxa
-
研究警告说 全球生物多样性可能比以前认为的还要糟糕
一项新的研究警告说,由于当前的生物多样性评估未能考虑到土地突然变化的长期影响,全球生物多样性的状况可能比以前认为的要糟。萨塞克...
-
结石清除可帮助一半的UTI复发患者
根据发表在《泌尿外科杂志》 10月号的一项研究,可以将一半的复发性尿路感染和无症状性肾结石患者通过结石摘除术消除感染。来自克利夫兰诊
-
国产优质轻客江铃特顺 性价比碾压大通V80
随着大众消费观念的转变,不少活跃在商用领域的车型,纷纷被家用市场所接受。这种发展趋势,也令各大车企在研发制造时有所创新,将多元...
-
福田区第二十届青少年科技节(创客节)暨第三届STEM教育嘉年华盛
12月11日上午,福田区第二十届青少年科技节(创客节)暨第三届STEM教育嘉年华在福田区科技中学开幕。本次活动由中共深圳市福田区委员会、深
-
研究显示肠道微生物如何影响胃流感
一项新的研究表明,肠道微生物可以根据首次感染的肠道位置,调节诺如病毒感染的严重程度(胃流感,或冬季呕吐病毒)。这项研究于2019年11...