台湾药华医药Besremi获欧盟批准
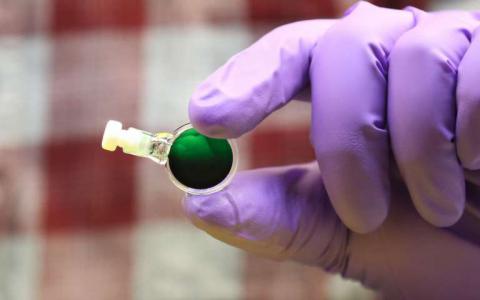
台湾药华医药(PharmaEssentia)与AOP Orphan制药公司近日联合宣布,欧盟委员会(EC)已批准Besremi(ropeginterferon alfa-2b)作为一种单一疗法,用于治疗不存在症状性脾肿大的真性红细胞增多症(PV)成人患者。根据III期临床数据,此次批准,使Besremi成为欧洲市场首个也是唯一一个获批治疗PV并且与先前羟基脲暴露无关的药物。在欧洲,Besremi的营销授权持有人是AOP Orphan制药公司。

药华医药首席执行官Kochung Lin博士表示,“我们很高兴现在有了一种获得批准的PV 新疗法。PV患者在发病早期迫切需要有效的治疗方案,因为不理想的疾病控制会导致严重的心血管并发症。”
Besremi将作为一种注射用溶液装在预充注射笔内(250微克/0.5毫升,500微克/0.5毫升)。Besremi的活性物质是药华医药发现并在中国台湾台中科学园根据PIC/S cGMP 规范制造的ropeginterferon alfa-2b。该工厂于2018年1月通过欧洲药品管理局(EMA)的GMP认证。
欧盟委员会的批准适用于所有28个欧盟成员国以及冰岛、挪威和列支敦士登。药华医药独家授权AOP Orphan在欧洲、独联体和中东市场开发和商业推广ropeginterferon alfa-2b,用于治疗PV、其他骨髓增殖性肿瘤(MPN)和慢性髓性白血病(CML)。
ropeginterferon alfa-2b是一种新型长效型单一异构体单聚乙二醇化脯氨酸干扰素(>98%,ATC L03AB15),具有改善的药代动力学特征,并已证明耐受性和便利性。该药每2周给药一次,或在长期维持治疗期间每4周给药一次,是首个获批用于治疗PV的干扰素产品。
ropeginterferon alfa-2b由药华医药发现并在一家位于中国台湾台中的工厂生产,该工厂于2018年1月通过EMA的cGMP认证。在美国、欧盟和瑞士,ropeginterferon alfa-2b均被授予了治疗PV的孤儿药资格。
真性红细胞增多症(PV)是一种源于骨髓中致病干细胞的癌症,导致红细胞、白细胞和血小板的慢性增加。这种疾病可能引发心血管并发症,如血栓和栓塞,甚至转化为继发性骨髓纤维化或白血病。虽然PV背后的分子机制仍有待深入研究,但目前的结果指向一组获得性突变,其中最重要的是Janus激酶2(JAK2)的一种突变形式:JAK2V617F。
推荐内容
-
蓝藻研究检查氮饥饿期间的细胞结构
利用非破坏性中子散射技术,科学家们正在研究称为蓝细菌的单细胞生物是如何产生氧气并通过光合作用获得能量的。华盛顿大学圣路易斯分校...
-
根据单细胞分子研究进行生物学教育
随机过程通常以随机的方式呈现,即不可预测的事件。这种框架模糊了这样一个现实,即随机过程虽然在个别事件层面上或多或少是不可预测的...
-
掌门1对1作为全球在线教育优秀案例登上世界教育创新WISE峰会舞台
第九届世界教育创新峰会(以下简称WISE)在卡塔尔首都多哈闭幕,本届大会集中展示了全球领先的教育创新成果。其中,中国K12在线一对一全科辅
-
一种可以加快基因组分析速度的软件
由A * STAR新加坡基因组研究所(GIS)和生物信息学研究所(BII)的研究人员领导的国际科学家团队开发了SIFT 4G(基因组SIFT) - 一种可以加
-
基因编辑工具CRISPR重新用于开发更好的抗生素
威斯康星大学麦迪逊分校的研究人员和他在加利福尼亚大学旧金山分校的合作者重新利用基因编辑工具CRISPR来研究特定抗生素靶向的基因,提供如
-
研究人员发现RNA-seq技术产生的数据经常存在技术偏差
研究数据的可重现性是实验生物学面临的一大挑战 随着基因组规模技术产生的数据的复杂性增加,这一关切变得越来越令人担忧。 RNA-seq...
-
北京荣盛众藏文化“东方墨彩-齐聚马来”中马艺术联展在马来西亚吉
2018年11月17日应马来西亚华人商会、马来西亚华人企业家联合会之邀,汇聚东方艺术,齐聚马来西亚,马来西亚华人商会、马来西亚华人企业家联合
-
黄酮类化合物可以显著降低患阿尔茨海默氏症的风险
发表在《gorron neurology》上的一项新研究得出结论,到2020年1月,从安装中增加黄酮类化合物的摄入量,可以将阿尔茨海默氏症(AD)的风...
-
械字号面膜不存在的?还有哪些坑依旧隐蔽
近年来,随着国民收入和大众对美的追求,各类医疗美容项目逐渐变得火热,之配套的产品也纷纷出现在消费者面前,械字号面膜正是随着这波...
-
研究人员向了解生命如何进化又迈进了一步
生物学的一个基本问题是解释生命如何进化。我们如何从益生元汤中的简单化学反应中获得动物和植物?解释生命的关键一步是大约40亿年前,我们