口服新药seladelpar获得FDA突破性疗法认定
近日,美国FDA授予CymaBay Therapeutics公司的临床3期在研药seladelpar突破性疗法认定,用于与熊去氧胆酸(ursodeoxycholic acid,UDCA)联合用药治疗对UDCA反应不足的原发性胆汁性胆管炎(PBC)成人患者,以及作为单药疗法治疗无法耐受UDCA的PBC成人患者。

原发性胆汁性胆管炎是一种有潜在生命危险的肝脏自身免疫性疾病。由于免疫系统持续攻击胆管,胆汁流动受阻而淤积,毒性胆汁酸在肝内留存,可发展为肝纤维化、肝硬化和肝功能衰竭。其他临床症状还包括疲劳和瘙痒。在40岁以上的女性中,有千分之一患有PBC。
正在临床开发阶段的seladelpar属于强效选择性过氧化物酶体增殖物活化受体(PPARδ)激动剂。PPARδ表达在肝脏的多种细胞类型中,临床前数据表明,它对调控胆汁酸合成、炎症、纤维化过程的多种基因有调节作用。除了治疗PBC以外,CymaBay公司也在开展2b期临床试验,使用seladelpar治疗非酒精性脂肪性肝炎(NASH)患者。
目前,CymaBay公司正在为seladelpar治疗PBC的全球性3期研究招募对UDCA应答不足或对UDCA不耐受的患者。名为ENHANCE的随机,含安慰剂对照的3期临床研究采将评估seladelpar的安全性和有效性,以52周后测量的应答患者比例作为主要终点。若患者碱性磷酸酶(AP)水平低于正常值上限的1.67倍,比基线降低15%以上且总胆红素水平正常,则视为产生应答。
获得FDA突破性疗法认定的在研药物需要有初步临床证据表明,至少一个临床关键性终点显著优于现有疗法。此次seladelpar获得认定,基于2期临床试验的概念验证。初步结果表明,从病情发展的重要指标AP水平的降低程度来看,新疗法相比现有疗法有显著改善。
“我们很高兴FDA认可seladelpar作为治疗PBC的潜在突破性疗法,这意味着认可PBC是一种迫切需要新疗法的严重疾病,” CymaBay Therapeutics的首席监管合规官(Chief Regulatory and Compliance Officer)Klara Dickinson先生表示:“我们期待通过与监管机构的密切合作来完成seladelpar的开发项目,以这些认定为契机,加速为PBC患者提供创新的治疗方案。”
推荐内容
-
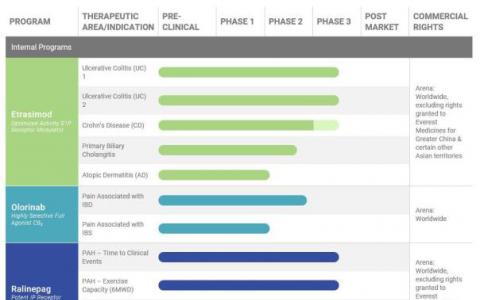
United Therapeutics 预付8亿美元买下在研治疗肺动脉高压药物ralinepag
今日,Arena Pharmaceuticals与United Therapeutics达成一项全球许可协议。United Therapeutics以8亿美元的预付款,未来4亿美元的里程碑
-
为什么这么多人不开实体店,而选择做赞播优鲜社区新零售?
先看这样一组数据:实体店倒闭率仍在攀升,开业半年后的存活率,不超过50%;开业一年后的存活率,不超过20%;开业三年后还存活的,低于1%。
-
2019年百亿大并购或将挫伤生物技术公司
2月25日晚,丹纳赫宣布214亿美元全现金收购GE生物医药板块业务,给9个月来的传闻画上了句号。同日,罗氏官网正式宣布将斥资43亿美元收购Spa
-
猎犬和狼共用寄生虫
灰狼是各种寄生虫的寄主。德国森林中灰狼的存在对猎犬的寄生虫负担几乎没有影响。这一令人欣慰的结论是在柏林的莱布尼茨动物园和野生动...
-
研究人员首次观察到快速弹弓细胞运动
通过向前弹射,人体细胞的传播速度比以前记录的速度快五倍以上。密歇根大学的研究人员观察了生物工程3D支架的运动,该支架模拟基质组织 -
-
分子魔术贴有助于照亮DNA修复
利用一块分子魔术贴将发光探针连接到蛋白质分子上,卧龙岗大学(UOW)的研究人员揭开了一个重要蛋白质如何修复细菌中受损DNA的神秘面纱,这对
-
飞蛾甚至其他动物都依赖于神经尖峰的精确定时
从可能在风中跳舞的花朵中提取花蜜需要大脑和肌肉之间精确的毫秒级时间。通过捕获并分析以这种花蜜为食的鹰蛾(Manduca sexta)的翼状肌肉发
-
研究发现蚊子不仅会产卵还会在干旱期间解渴
当它炎热干燥时,蚊子就像你的清爽味道一样。辛辛那提大学的生物学家发现,雌性蚊子不仅能够获得产卵所需的蛋白质,还能在干旱期间解渴...
-
新方法降低细胞因子疗法的毒性
尽管它们有潜力,但细胞因子尚未成功地发展成有效的癌症疗法,因为它们对健康组织和肿瘤都具有高毒性。根据最近的一项研究,这可能会发...
-
突变的蛙基因排斥食肉动物
博士后研究员AndrésPosso-Terranova和他的前任主管JoséAndrés已经发现了一个名为MC1R的基因可以控制这些有毒青蛙皮肤