教你2型糖尿病患者血糖控制及ClinGen —临床基因组资源
退伍军人事务糖尿病试验先前显示,与标准疗法相比,强化降糖治疗并未显着降低1791名退伍军人中主要心血管事件的发生率(中位随访时间为5.6年)。我们报告了研究参与者的进一步随访。
方法
临床试验结束后,我们追踪参与者,使用中央数据库确定手术,住院和死亡(完整队列,并随访92.4%的参与者的数据)。大多数参与者都同意通过年度调查和定期图表审查的方式收集更多数据(调查队列,随访率为77.7%)。主要结果是发生第一次重大心血管事件的时间(心脏病发作,中风,新发或恶化的充血性心力衰竭,截肢缺血性坏疽或与心血管相关的死亡)。次要结果是心血管疾病死亡率和全因死亡率。
结果
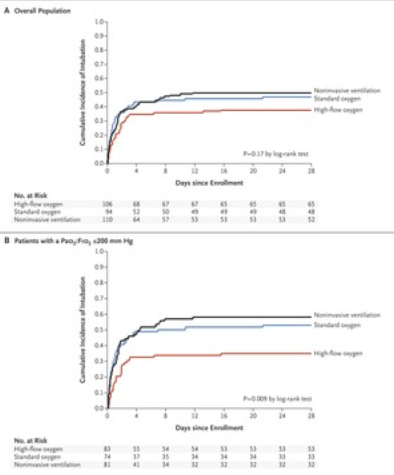
强化治疗组与标准治疗组之间糖化血红蛋白水平的差异在试验期间平均为1.5个百分点(中位水平为6.9%对8.4%),到试验后3年下降至0.2-0.3个百分点结束了。在9.8年的中位随访中,强化治疗组的主要结局风险显着低于标准疗法组(危险比,0.83; 95%置信区间[CI],0.70至0.99; P = 0.04),每1000人年中8.6个重大心血管事件的绝对风险降低,但心血管疾病死亡率没有降低(危险比,0.88; 95%CI,0.64至1.20; P = 0.42)。总死亡率没有明显降低(强化治疗组的危险比为1.05; 95%CI为0.89至1.25; P = 0.54;中位随访时间为11.8年)。
结论
经过近10年的随访,被随机分配为强化血糖控制5.6年的2型糖尿病患者每1000人年的主要心血管事件比分配标准治疗的患者少8.6次,但在2000年中未见改善整体生存率。
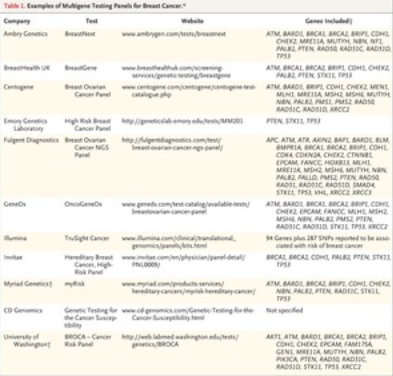
检时发现患者患有肥厚型心肌病。患者的家人根据原始研究出版物中的一项研究进行了基因检测,结果表明该病的“可能是致病性”变异。考虑到疾病的主要遗传因素和心脏猝死的风险,应对其他家庭成员进行遗传变异测试以确定他们的风险。几位家庭成员的检测结果均为阴性,并被告知他们没有肥厚型心肌病和猝死的危险,而那些检测结果为阳性的人则被告知需要定期接受超声心动图监测。五年后,在一位基因型阳性家庭成员的常规门诊期间,心脏病专家向数据库查询有关遗传变异的当前知识,并发现该变异现在被另一家使用最新推导的人口频率数据的实验室解释为“可能是良性的”。在受影响的家庭成员上启动了新的涉及肥厚型心肌病的其他基因的检测小组,并发现了一个确定为致病性的不同变异体。重新测试了家庭成员,现在发现以前测试为阴性的一位成员对此新变体是阳性的。立即进行临床检查即可发现心肌病的证据,并植入了心脏内除颤器以减少心脏猝死的风险。在受影响的家庭成员上启动了新的涉及肥厚型心肌病的其他基因的检测小组,并发现了一个确定为致病性的不同变异体。重新测试了家庭成员,现在发现以前测试为阴性的一位成员对此新变体是阳性的。立即进行临床检查即可发现心肌病的证据,并植入了心脏内除颤器以减少心脏猝死的风险。在受影响的家庭成员上启动了新的涉及肥厚型心肌病的其他基因的检测小组,并发现了一个确定为致病性的不同变异体。重新测试了家庭成员,现在发现以前测试为阴性的一位成员对此新变体是阳性的。立即进行临床检查即可发现心肌病的证据,并植入了心脏内除颤器以减少心脏猝死的风险。
图1.
15,000个先证者的孟德尔疾病测试得出的变异直方图。
在过去的25年中,在破译人类疾病的遗传基础方面已经取得了重大进展,并且在遗传水平上已经了解了超过5000种孟德尔疾病。1尽管这对于我们了解人类疾病的生物学特征而言是一项非常重要的成就,但由于缺乏已知的现有大量人类遗传变异的公开可用且准确的解释,这些发现与临床护理的整合面临着严峻挑战。 。在人类基因组中发现了超过8000万个遗传变异,2对于大多数人来说,我们对它们在人类健康和疾病中的作用尚无明确的了解。因此,即使患者携带与高渗透性遗传疾病相关的基因变异,我们仍可以远离患者基因组并轻松解释其患病风险。孟德尔基因中鉴定出的大多数变体的稀有性(图1))使得难以解读此类变体对基因功能的影响;最罕见的变体被标记为“不确定意义的变体”。导致我们缺乏一致,清晰和临床相关的人类遗传变异注释的最后一个因素是所谓的筒仓效应,在这种筒仓效应中,各种商业和学术实体都保持孤立状态。 ,有时是专有的变体解释数据库,从而防止共享可能使患者,家庭,医疗保健提供者,诊断实验室和付款人受益的关键知识。
根据对国家生物技术信息中心(NCBI)的ClinVar变异数据库提交资料的分析3,我们发现多个临床实验室对同一变异的重要性的解释可能有所不同,因此至少有一个如上例所示,解释必定是错误的,因此可能导致不适当的医疗干预。孤立的实体之间的健康竞争已不足以推动我们对人类变异的理解,并且如果不共享数据,患者的护理可能会受到影响。如果社会要了解人类基因组变异并在临床护理中获得其收益,那么巨大的合作努力将是积累足够数据并分配重要审查责任的唯一途径。
在过去的几年中,合作的努力显示了将数据提交到公共数据库以促进遗传发现的有效性。例如,如果不鼓励公开发布数据,当前的人类参考序列将是不可能的。4同样,对于验证全基因组关联研究5至关重要的复制取决于从越来越大的同类人群中获取数据以鉴定越来越少的等位基因(或效应大小较小的常见等位基因)。该领域从数据共享文化中受益匪浅,如今,已经鉴定了300多个复杂性状的遗传基因座,并在2000多篇文章中进行了报道,其中许多是通过高度可重复的全基因组关联研究得出的。6-8癌症遗传学界还组织了数项重大工作,包括《癌症基因组图集》9和国际癌症基因组协会[ 10],其中对从肿瘤和正常组织获得的基因进行了测序,并将结果数据存入数据库以识别复发性变异与不同类型的癌症相关。这些财团和研究大多数都集中在具有预定义参与实体的,仅在研究环境中获得的数据。为了使基因发现能够在医学上得到利用,提高基因测试的数据收集和共享标准,以及定义用于基因组和表型变异的临床注释和解释的系统方法,同样重要。
推荐内容
-
11月18日南京市疫情最新消息公布 南京栖霞助力湟中疫情防控
小编在这里提醒大家,疫情期间,尽量做到非必要不出行,如果一定要出行,要关注交通旅游信息,同时还要注意错峰出行,全程做好防护,尽...
-
医保二次报销需要什么条件2021 医保二次报销比例条件和新规定
众所周知,医保给老百姓带来实实在在的便利,让患者真正做到了看得起病。那么,你知道医保二次报销需要什么条件吗?根据规定,使用医保二次
-
北大女生自杀后续 包丽自杀后235天案情有何进展?
【导读】pua想必大家现如今已经对于这个词不再陌生了,近几年被pua男或者说是pua女的时间屡见不鲜,近来北大女生自杀后续公布了吗?包丽自杀
-
乐言道歉是怎么回事 姿态举报乐言卢崛利用英雄联盟BUG上分
【导读】今日凌晨,VG战队选手乐言Leyan(卢崛)排位利用BUG上分,姿态向官方人员举报!这波乐爷应该会禁赛吧,对此刚刚乐言道歉回应都说了什
-
Moderna公司21个研发管线与5亿美元的IPO秒杀同行
近日,美国网红企业Moderna向美国证券交易委员会递交了IPO申请书S-1,拟在纳斯达克全球精选板块进行5亿美元的首次公开募股。这也意味着,此
-
11月8日四川成都疫情最新消息公布 成都两地调整为中风险地区
温馨提示:一旦出现发热、干咳、乏力、鼻塞、流涕、咽痛、嗅觉味觉减退、结膜炎、肌痛和腹泻等症状,应及时按规范程序就诊,并主动告知1...
-
8月24日韩国疫情最新实时数据公布 韩国昨日新增1509例新冠确诊病例
韩国新增1509例新冠确诊病例,连续49天保持四位数。那么,对于韩国疫情的这个话题,今天的你是否也在关注着?具体什么情况?下面跟小编一起来
-
涿州疫情3月9日至11日全员还查核酸吗?河北保定涿州疫情解封日期
【导读】涿州疫情什么时候解封?现在涿州疫情管控什么情况?据消息显示,根据河北涿州市3月9日公布的疫情数据,河北涿州新增3例本土确诊病例
-
南昌新冠肺炎疫情最新消息:南昌新增1例无症状感染
【导读】今日南昌新冠肺炎疫情最新消息,据悉南昌新增1例无症状感染者,如今又出现一例境外输入无症状感染者,这告诉大家虽然我国疫情趋向
-
官方回应家长到指定书店买教辅 已紧急叫停购买行为且问题部分属实
最近一则家长到指定书店买教辅的新闻引起网友关注和讨论,针对老师推荐家长到指定书店购买教辅一事,当地教体局最新回应称,已紧急叫停...