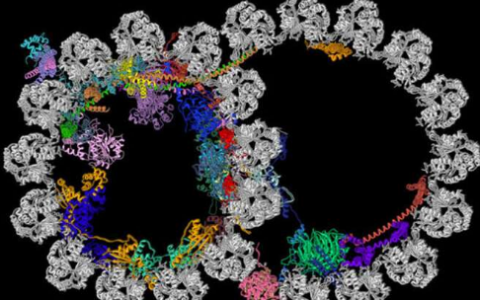
实验性疫苗诱导抗体 可中和多种艾滋病毒紧张局势
斯克里普斯研究中心和非营利疫苗研究组织IAVI的科学家开发的一种实验性艾滋病毒疫苗已经达到了一个重要的里程碑,它可以诱导抗体来中和各种艾滋病毒紧张局势。

在兔子身上进行的测试显示,这些“广泛中和”抗体(bnAbs)至少针对了病毒中的两个关键部位。研究人员普遍认为,如果疫苗要对这种不断变化的病毒提供强有力的保护,就必须将bnAbs诱导到艾滋病毒的多个位点。
在免疫方面出现的有希望的结果表明,研究人员离研制出一种有效的艾滋病毒疫苗又近了一步。
这是对这一原则的初步证明,但也是一个重要的证明,我们现在正在努力完善这一疫苗接种项目。
理查德·怀亚特博士,斯克里普斯研究免疫学和微生物学系高级教授
根据联合国艾滋病规划署的数据,全世界大约有3500万人死于由艾滋病毒感染引起的免疫缺陷综合症艾滋病。另有3800万人感染了艾滋病毒。抗病毒药物可以使艾滋病毒感染者存活下来,降低他们将病毒传播给他人的能力,但这些药物使感染变得模糊,必须无限期服用。研究人员长期以来一直认识到,有必要消除艾滋病毒这一主要公共卫生威胁。
艾滋病毒的快速变异率和其他规避免疫攻击的机制使其成为疫苗设计人员极其困难的目标。但是怀亚特和他的团队进行的测试证实,疫苗接种可以诱导提供广泛的艾滋病毒保护所需的抗体类型。这些bnAbs,正如疫苗专家所称,可以中和多种艾滋病毒紧张,因为它们连接到病毒的关键部位,而这些部位在不同的紧张程度上变化不大。感染艾滋病毒bnAbs产品的人有时作为抗体反应的一部分,但很少,而且通常在感染确立很久之后。艾滋病毒疫苗设计者面临的主要挑战是找到刺激免疫系统的方法——在大多数或所有个体中——使bnAbs攻击病毒中的多个脆弱部位,以保护其免受高比例的艾滋病毒紧张。
怀亚特及其同事的疫苗接种项目的核心是一种基于艾滋病毒“Env”蛋白的病毒模仿蛋白。通常情况下,环境病毒蛋白的多个布什样副本分散在每个球形艾滋病毒粒子的表面。Env中的每一种蛋白质都包含一种分子机制,使其能够连接到免疫细胞中被称为CD4的受体,并将该受体用作细胞中分解的门户。研究人员设计了一个版本的Env,该版本模拟了实际环境中的基本结构,因为它在用作疫苗时相当稳定。现在,它以一种类似于hiv病毒的真实粒子的方式,制造出了由与脂肪相关的分子“脂质体”量身定做的病毒合成球体,这些分子被设计的Env蛋白致密填充。
在一种天然的艾滋病毒环境蛋白中,由糖相关分子组成的树状体被称为葡聚糖的帮助保护剂,通常是CD4,它对免疫攻击具有最高的强制性局部重要性。作为对“天狼星”的初步免疫,研究人员使用了Env版本,其中CD4位点附近的这种糖化保护剂部分被移除。
怀亚特说:“我们的想法是改善这个地方的暴露情况,从而在一开始就刺激他产生广泛的抗体反应。”
在随后的48周内,助推器免疫使用恢复糖原的Env蛋白来选择针对强制CD4位点但也可以通过该保护剂获得的抗体。助推器注射中的Env蛋白也是基于不同艾滋病毒张力的混合物,通常促进抗体对这些张力之间没有差异的Env结构的反应。
该小组在接种策略后接种了12只兔子,并将结果与只接受单一糖保护版本Env的对照组进行了比较。他们发现他们的疫苗策略有更好的反应,其中5只兔子产生的抗体可以中和多发性艾滋病毒。
研究人员分析了反应最强烈的兔子抗体,并确定了两种不同类型的bnAb。其中一种被称为E70,如预期的那样,以一种不同寻常的方式阻塞了强制的CD4位点——部分原因是附着在保护聚糖上。另一个,1C2,在Env中遇到了一个不同但已知的脆弱点,即复杂蛋白的两个关键片段之间的关系。1C2抗体的堵塞显然会破坏Env,因此它可能不再协商将艾滋病毒输入宿主细胞。这种抗体还具有不同寻常的中和宽度,阻碍了208种不同的艾滋病毒分离株的87%。
怀亚特说,找到一个重要的证据表明,如果以正确的方式接种艾滋病毒疫苗,就可以实现将bnAbs诱导到病毒中多个位点的目标。
科学家们正在继续在小型动物模型中测试和改进他们的疫苗接种策略,并希望最终在猴子和人类中进行测试。
推荐内容
-
母婴基因如何影响出生体重
同类研究中规模最大的研究已经引发了关于母亲和婴儿基因如何影响出生体重的复杂关系的新见解。该研究发表在Nature Genetics上,确定了我们
-
文在寅被扔鞋让人大跌眼镜 文在寅是韩国罪人?
我们都知道韩国总统文在演是一位非常优秀的总统,但是近来文在寅被扔鞋让人大跌眼镜,到底是什么样原因竟然会让深受人爱戴的总统被丢鞋呢?
-
河南22岁女网红美美徒步西藏怎么了?河南22岁女网红美美的死因是
22岁女网红徒步西藏遇难,曾在最后直播中痛苦呻吟,出事原因成疑。那么,对于22岁女网红徒步西藏遇难的这个话题,今天的你是否也在关注着?
-
2月2日广东惠州疫情实时信息公布 惠州新增1例确诊病例,为31
广东惠州新增1例新冠肺炎确诊病例 为31日深圳确诊病例的密接。据广东惠州卫生健康局消息,广东省惠州市新增1例新冠肺炎确诊病例。病例:郑
-
科学家揭开细胞鞭状延伸的奥秘
纤毛或鞭毛(细胞鞭状附件)执行维持身体健康所需的各种任务。当纤毛失灵时,后果可能是毁灭性的,导致一系列问题,从失明到肺和肾脏疾病...
-
张哲瀚和黛薇夫人事件怎么回事始末介绍 黛薇夫人是谁什么来头
黛薇夫人是谁怎么了?与张哲瀚关系密切个人立场引发热议。那么,对于黛薇夫人是谁的这个话题,今天的你是否也在关注着?具体什么情况?下面跟
-
刘鑫刘暖曦现在怎么样了家里有钱吗个人背景资料起底 刘暖曦江
刘鑫是谁?据消息显示,刘鑫,女,中国山东青岛市城阳区苇芦村人。 2014年毕业于山东泰山学院 。 2014年到日本语言学校,2016年入读日本
-
全日食期间的超人夜景研究提供了生物学解释
如果你有幸见证了最近的日全食,那么你可能已经注意到了令人惊讶的事情。夜晚很黑,但人们和物体比典型的无月夜更容易看到。俄亥俄州立...
-
8月21日南京疫情最新实时消息公布 南京全域公共交通昨日逐步恢复
疫情未结束,防范措施不可松懈。勤洗手。使用肥皂或洗手液并用流动水洗手,用一次性纸巾或干净毛巾擦手。双手接触呼吸道分泌物后(如打喷嚏
-
海参 属海参纲是生活在海边至8000米的海洋棘皮动物
核心提示:海参,属海参纲(Holothuroidea),是生活在海边至8000米的海洋棘皮动物,距今已有六亿多年的历史,海参以海底藻类和浮游生物为食