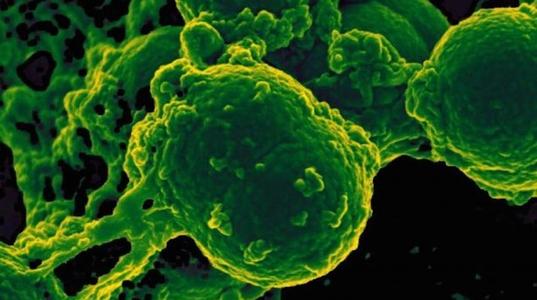
CRISPR基因组编辑在小鼠中阻止三阴性乳腺癌
波士顿儿童医院和东北大学的科学家们开发了一种CRISPR基因组编辑系统,可以抑制三阴性乳腺癌(TNBC)的生长。一项校长证明研究表明,设计用于靶向已知癌症基因的纳米脂凝胶递送的CRISPR系统使小鼠模型中的肿瘤生长停止了77%,没有任何对正常组织有毒性的证据。“我们的研究结果提供了体内CRISPR基因组编辑可以阻止TNBC肿瘤进展的实验证据,”该研究小组在他们发表在“ 美国国家科学院院刊”上发表的论文中写道,该论文标题为“ 三阴性乳腺肿瘤的治疗性基因组编辑 ” 使用非阳离子和可变形纳米脂凝胶。“
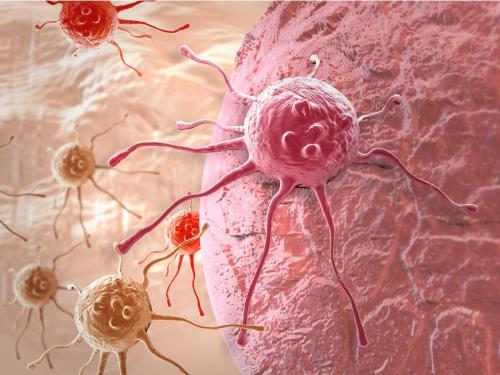
研究人员和研究员彭国博士以及波士顿儿童医院血管生物学项目主任Marsha Moses博士领导的研究人员解释说,TNBC是所有乳腺癌类型中最具攻击性的,预后最差。TNBC在50岁以下的女性,非洲裔美国女性和携带BRCA1基因突变的女性中发生率更高。“据估计,2019年美国有超过32,000名患者被诊断为TNBC,占所有新发乳腺癌病例的12%,”该团队写道。“TNBC的极端侵袭性和转移性,加上较少的治疗选择,导致所有乳腺癌亚型中最严重的死亡率,凸显了治疗TNBC的新型精确药物的迫切和未满足的临床需求。”
虽然CRISPR基因组编辑显示有希望作为包括癌症在内的遗传疾病的潜在治疗或甚至治愈,但在实践中,大多数临床关注的CRISPR研究都集中在由单个基因缺陷引起的直接单基因疾病上。“研究人员指出,体内CRISPR基因组编辑对更复杂的多基因疾病(如TNBC)的治疗益处尚不清楚。” “到目前为止,尚未研究过体内CRISPR基因组编辑作为TNBC的靶向治疗药物。”
将CRISPR基因组编辑的潜力转化为治疗平台的部分原因在于缺乏有效的传递系统。病毒介导的CRISPR元件的递送不适合携带大的有效载荷,并且可能潜在地引起非靶细胞的副作用。另一种方法涉及将CRISPR有效负载包封在阳离子聚合物或脂质纳米颗粒内,但这也可能导致毒性,并且CRISPR元件可能被捕获在细胞内体内,或在到达靶细胞之前被分解。
波士顿儿童医院团队开发的方法将CRISPR系统封装在由无毒脂肪分子和水凝胶组成的柔软非阳离子纳米脂凝胶内。然后在纳米脂凝胶表面上铺上针对ICAM-1的抗体,ICAM-1是由摩西实验室在2014年鉴定的一种蛋白质,作为TNBC的新药物靶标。初始细胞摄取研究表明,ICAM-1抗体有效地将含有CRISPR的纳米脂凝胶颗粒引导至TNBC细胞。进一步的研究表明,与较硬的纳米颗粒不同,软肿瘤靶向纳米脂凝胶(tNLG)颗粒可以很容易地与肿瘤细胞膜融合,并将CRISPR有效负载直接传递到细胞内。“... tNLGs可以选择性识别TNBC细胞并将其与正常乳腺细胞结合,这可能会降低其体内非特异性毒性,与我们之前使用ICAM1作为TNBC靶标的研究结果一致,“作者说。“...可变形的tNLGs可以在体外更有效地破坏肿瘤内皮屏障,而不是它们的僵硬对应物,这反过来可以提高其体内表现。”作为第一作者,郭评论说,“使用软颗粒可以让我们穿透肿瘤更好,没有副作用,并且货物更大。我们的系统可以显着增加CRISPR的肿瘤传递。“ 和更大的货物。我们的系统可以显着增加CRISPR的肿瘤传递。“ 和更大的货物。我们的系统可以显着增加CRISPR的肿瘤传递。
为了利用该技术作为TNBC的潜在治疗策略进行概念验证测试,研究人员设计了CRISPR系统以靶向Lcn2,这是他们之前发现的一种已经发现的癌症基因,它可以积极促进乳腺癌的进展和转移,从而产生tNLG -Lcn2KO纳米脂凝胶颗粒。在过量表达Lcn2的人TNBC细胞系中的测试证实,tNLG-Lcn2KO系统能够“有效且高效地进行CRISPR基因组编辑”,并且在基因转录物和蛋白质水平上抑制Lcn2的表达。通过抑制上皮至间充质转换(EMT),促进乳腺肿瘤进展和转移的机制,TNBC细胞中Lcn2的CRISPR敲低导致肿瘤细胞侵袭性降低和迁移倾向。
他们接下来将tNLG-Lcn2KO注射到携带TNBC的小鼠中,并发现在给药后24小时内,ICAM-1引导的颗粒特异性地归巢于TNBC,其水平比使用对照纳米脂凝胶颗粒高1.7倍。他们指出,tNLG-Lcn2KO在小鼠肿瘤中的积累水平“显着高于常规纳米药物的平均肿瘤积累”。
为了评估系统的治疗潜力,每周接受含有TNBC的小鼠tNLG-Lcn2KO纳米脂凝胶颗粒注射4周,并使肿瘤继续生长另外4周。结果显示,与对照动物相比,tNLG-Lcn2KO治疗使肿瘤体积减少77%,肿瘤重量减少69%。与接受假处理的小鼠的结果相比,体内编辑效率为约81%,导致tNLG-Lcn2KO治疗组中lcn2蛋白水平显着降低。“这些体内结果提供了实验证据,即tNLGs有效的体内CRISPR基因组编辑可以产生针对TNBC肿瘤生长的有效和特异性治疗益处。”
令人鼓舞的是,没有证据表明在包括肝脏,脾脏和肾脏在内的器官中存在与治疗相关的毒性,这表明“tNLG的纳米制剂相对安全地用于体内CRISPR基因组编辑”。
作者得出结论,他们的原理证明研究表明,tNLG制剂具有“将CRISPR基因组编辑转化为癌症治疗中的新型精确医学的有希望和广泛的潜力。”使用tNLG作为平台传递也应该是可行的。他们建议,使用其他靶标靶向TNBC以引导纳米脂凝胶颗粒进入体内TNBC肿瘤。他们指出,不同的TNBC癌基因,如PIK3CA,WNT和Notch,也可作为Lcn2阴性TNBC亚型的替代基因组编辑靶点。“我们的系统能够以精确和安全的方式为肿瘤提供更多的药物,”摩西总结道。
推荐内容
-
今日说法周进严坤案件最新详情后续:周进痛哭的原因是什么?周进
网购迷药、制造车祸杀妻!警方发现,这已经是第二次…… 据消息显示,近日就有一则关于男子制造2次车祸杀妻骗保被判死刑的消息引起了网上...
-
实验性抗生素治疗致命的MRSA感染
《美国肾脏病学杂志》上的一项研究提出了一种新的治疗方法,用于治疗继发于慢性心力衰竭的慢性肾脏疾病的发展,这种疾病称为2型心肾综合征
-
食锈末世录小说女主叫什么?食锈末世录更新时间是什么时候?
今日小编为大家带来一则关于食锈末世录漫画的相关文章。如果您喜欢这篇文章,请大家点个赞,以示鼓励。喜欢我就关注一下哦,谢谢。食锈...
-
丰巢高管出门回应称不会放弃超时收费 5年亏损超20亿
近段时间快递行业就数丰巢最引人关注了,因丰巢云柜超时收费引发了不少的口水战,刚刚丰巢高管出门回应称不会放弃超时收费?那么你你觉得丰
-
新技术照亮了无法在实验室培养的微生物
在斯坦福大学,研究人员使用一种新的微流体分析系统从两个黄石国家公园温泉的样本中提取29种新的微生物基因组(完整的遗传物质)。他们在保留
-
李赛高是谁什么职业个人经历背景资料起底 佤邦李赛高的视频瓜
【摘要】号称百万粉丝的网红李赛高账号在平台上消失。其实真的是骗子的身份了!据消息显示,这位自称是远征军后代的网红李塞高,其实是缅甸
-
满洲里新增本土无症状感染者1例 内蒙古满洲里新增患者多次乘公交车
【导读】现在又到了冬季,防病毒形势较为严峻,怎么战胜病毒呢?近来内蒙古满洲里疫情备受关注,据悉今日满洲里新增本土无症状感染者1例...
-
今天股市行情最新数据公布 6月21日股市开盘情况汇总
今天股市行情最新消息,6月21日股市开盘情况是什么?而对于今天股市行情的这个话题,今天的你是否也在关注着?究竟什么情况?6月21号消息,今
-
芒果超媒今天怎么了最新消息2021 芒果超媒今天股价为什么大跌?
【导读】你知道芒果超媒吗?据消息显示,芒果超媒股份有限公司于2005年12月28日成立。法定代表人张华立。2019年9月1日,2019中国服务业企业5