超越基因来解释血细胞的命运
科学家经常谈论细胞命运和控制基因表达机制(转录因子,染色质重塑等)的承诺。但是,通过研究罕见的遗传性血液病Diamond-Blackfan贫血症(DBA),由麻省理工学院和哈佛大学广泛研究所以及Dana-Farber /波士顿儿童癌症和血液疾病中心(DF / BC)的研究人员领导的团队发现了控制红细胞是否实现完全发育的惊人机制,与表达无关。
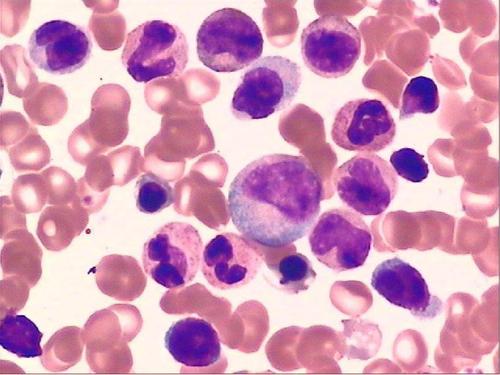
在纸单元,团队透露,在红血细胞的祖先,蛋白生产核糖体的可用数量来进行翻译,但那些不化妆核糖体,是他们的发育命运的主要驱动力。
红细胞从称为红细胞祖细胞的未成熟祖先发育而来。DBA患者携带的这些前体远少于正常人。研究人员早就知道DBA细胞携带与核糖体相关的基因突变,核糖体是读取mRNA转录物并构建编码蛋白质的杂交RNA /蛋白质分子机器。
认识到DBA为研究核糖体是否影响细胞命运提供了“自然实验”,研究生Rajiv Khajuria和Broad和DF / BC的准成员Vijay Sankaran与广泛的蛋白质组学平台,Broad核心研究所成员Aviv Regev的实验室和创始人Eric Lander和其他合作者检查正常和DBA血液祖细胞中的基因表达,蛋白质产生和核糖体丰度和组成。
研究小组发现携带DBA相关突变的祖细胞携带的核糖体比正常少得多。它们减少的核糖体含量与蛋白质产生的有趣变化相吻合。研究小组发现,核糖体缺陷细胞将某些mRNA转化为蛋白质的效率远低于正常水平。那些mRNA倾向于短,由在正常血液前体中大量表达的基因产生,并且具有通常与非常有效的翻译相关的分子特征。(值得注意的是,该组包括用于红细胞发育的主控制开关GATA1的mRNA。)
总而言之,该团队的结果提供了一种诱导性的线索,这种线索可能在许多细胞类型中起作用,不依赖于表达的细胞命运机制。事实上,他们指出,核糖体问题引发了一系列疾病,包括某些神经发育障碍和各种先天性缺陷 - 这表明DBA可能只是划伤了表面。
推荐内容
-
11月30日呼伦贝尔市新巴尔虎右旗疫情消息公布 内蒙古新巴尔虎
内蒙古新巴尔虎右旗发现2例新冠病毒核酸检测阳性人员。据消息显示,11月30日,内蒙古呼伦贝尔市新巴尔虎右旗新型冠状病毒感染肺炎防控工作
-
何鸿燊去世 二太太跟四太太就要开始斗法了?
何鸿燊去世的消息传来!一生传奇的赌王何鸿燊去世,对他而言是一种解脱。几房把他当吉祥物,更关心的是财产分配,财产大战中二房胜出,而被
-
今日冬至是几点几分几秒?冬至南北都吃什么
想必大家都知道,冬至,又称日南至、冬节、亚岁等,兼具自然与人文两大内涵,既是二十四节气中一个重要的节气,也是中国民间的传统祭祖...
-
10月9日山东青岛疫情最新数据公布 青岛昨天新增境外输入确诊病
青岛10月8日新增境外输入确诊病例1例,为菲律宾籍船员。那么,对于山东青岛疫情的这个话题,今天的你是否也在关注着?具体什么情况?下面跟小
-
11月5日额济纳旗疫情最新消息公布 额济纳旗:将开展第四次重
额济纳旗:将开展第四次重点地区、重点人群新冠病毒核酸检测工作。据消息显示,当前疫情防控形势极其严峻复杂,为严防疫情输入和扩散,...
-
深圳中高风险地区有哪些最新名单公布 目前出深圳要48小时核酸
众所周知,深圳是一座大城市,每天都有无数人出出入入,但最近深圳出现不少本土确诊病例,且有几个小区被定为中风险地区。那么,目前进...
-
11月9日武汉疫情最新实时数据公布 湖北昨日新增境外输入无症状
自疫情爆发以来,想必大家对数据变化都十分关注,疫情传来好消息或坏消息都会关系到人们的生活,也会影响人们对疫情的心态。据最新消息显...
-
11月2日宁夏银川疫情最新数据公布 银川昨日新增本土确诊病例1例
宁夏疫情,要结束了吗? 宁夏疫情,要反弹了吗?据最新消息显示,刚刚就有一则关于宁夏11月1日新增新冠肺炎本土确诊病例1例的消息引起了网友
-
光控工具可用于揭示蛋白质功能的秘密
加州大学旧金山分校的科学家发明了一种技术,通过在蓝光照射下将它们分开,可以精确地,可逆地破坏特定细胞蛋白在微观尺度上的作用。研...
-
钱枫被爆性侵是怎么回事?钱枫结婚了吗恋爱史介绍
想必这两天,大家对于钱枫性侵一事是非常关注的,具体是什么情况呢?下面跟小编一起来了解下事件始末。24日下午,有账号为小艺希望坏人被惩