研究人员使用TACC超级计算机创建了基因编辑的第一个全原子模拟
在过去十年中最受关注的生物学突破之一是发现了基因组编辑工具CRISPR / Cas9,它可以改变DNA并可能消除许多遗传性疾病的根本原因。最初作为化脓性链球菌细菌的免疫系统的一部分被发现,CRISPR相关蛋白9(CAS9),在其天然状态下,识别外源DNA序列并使其失效。在细菌中,该系统用于靶向来自噬菌体的外来病毒DNA - 它已经通过其进化历史识别为敌人的DNA,并将其记录到其自身的DNA中。

CRISPR(具有规则间隔的短回文重复序列,发音为“crisper”)代表DNA片段,其包含短重复碱基序列,随后是来自先前暴露于外源DNA的短片段“间隔DNA”。该复合物由解开DNA的蛋白质组成,其他在特定位置切割双螺旋的蛋白质,以及能够识别细胞中敌人DNA的指导RNA。
研究这种古老免疫系统的研究人员意识到,通过改变指导RNA的序列以匹配给定的目标,它不仅可以用于切割病毒DNA,而且可以用于精确选择位置的任何DNA序列。此外,可以引入新的DNA切片以连接到新切割的切片。
该方法最初由Jennifer Doudna(加州大学伯克利分校)和Emmanuelle Charpentier(Umeå大学)构思和开发,并已用于培养细胞 - 包括STEM细胞 - 和受精卵中,以创建具有靶向突变的转基因动物,有助于研究遗传功能。CRISPR / Cas9可以同时影响许多基因,从而可以治疗涉及许多基因相互作用的疾病。
该方法正在迅速改进,并且有望在有一天应用于基础研究,药物开发,农业和治疗患有遗传疾病的人类患者。
然而,创建靶向CRISPR / Cas9突变目前是昂贵且耗时的,特别是对于大规模研究。该过程也容易出错,限制了其广泛使用。这些问题的部分原因在于缺乏对CRISPR / Cas9在分子水平上如何起作用的充分理解。
11月,由Jin Liu领导的北德克萨斯大学(UNT)的研究团队使用德克萨斯高级计算中心(TACC)的Maverick超级计算机,对Cas9催化的DNA裂解进行了首次全原子分子动力学模拟。
“ 自然科学报告”中报道的模拟揭示了Cas9 基因组编辑的过程。他们还帮助解决了关于切割的具体方面的争议:例如,编辑的确切位置以及Cas9是否产生钝端或交错结束的断裂以及DNA中的突出物。
“目前我们在治疗应用中如何使用它们存在很多问题。酶的特异性和效率并不高,”刘说。“将酶传递到基因编辑的位置也很困难。为了解决这些问题,首先,我们需要知道这种酶是如何起作用的。我们的研究为理解Cas9的机制奠定了基础。”
科学家之前通过X射线晶体学确定了Cas9处于非活动状态的结构,但基因编辑过程发生得如此之快,以至于没有实验技术可以捕获其状态变化并确切地确定其工作原理。使用分子动力学模拟 - 通过模拟大量原子在固定时间内的相互作用来研究分子动力学的方法 - 刘和共同作者Zhicheng Zuo,也在UNT,能够观察到Cas9酶的变化以飞秒分辨率捕获转换到系统的活动状态。
模拟包括Mg2 +离子,据信它可以诱导Cas9中的构象变化,因此它可以起作用。研究人员假设Mg2 +离子通过促进Cas9活性位点和DNA的接近而诱导构象变为活跃状态。
模拟刘和左在Maverick上运行包含280,000个相互作用的原子。根据刘的说法,最具挑战性的部分是有效地采样构造空间以定位活动状态。
“我们尽力提高模拟结果的可靠性,”刘说。“我们做了几个长200和300纳秒的轨迹,我们还做了几个60纳秒的短轨迹,以确保我们得到一致的结果。对于每种配置,我们至少进行了六次并行模拟。”
除了研究CRISPR / Cas9复合物如何变为活跃状态外,模拟还揭示了它剪断DNA的位置。
UNT药物科学助理教授刘说:“通常人们认为它被削减到一个位置,但没有明确的证据表明这一点。” “使用我们的计算方法,我们确定切割发生在另一个位置,这可能意味着这种酶可以以更可控的方式切割DNA。因此,通过这项工作,我们打开了设计更有效的酶的门,可以切割DNA以更具体的方式。“
他们的最终贡献回答了基因组编辑是否产生了直接的结尾或交错的结束 - 一个具有实际意义的未解决的问题。
CRISPR / Cas9切割双链DNA的两半。如果它在两条线上的相同位置切割,它将产生钝端; 如果它在略微不同的位置切割,它将产生交错的结束。他们的模拟表明CRISPR / CAS9产生交错的结束。
“这对于基因编辑非常关键,因为交错结束的DNA比钝端DNA更易控制,”她说。
UNT制药科学主席Iok-Hou Pang使用CRISPR / Cas9在他的实验室进行实验眼科研究。对于他目前和将来的研究,他都看到了更清楚地理解酶行为的价值。
“我的实验室一直在使用CRISPR / Cas9 基因编辑系统来敲除培养的小鼠视神经星形胶质细胞中的一种新蛋白质,”Pang说。“刘博士的工作将帮助我们理解酶系统与其底物之间的分子相互作用,并最终有助于提高其效率,这对于这种奇妙的分子技术非常有用。”
2015年,在国家科学院的支持下,全球科学家宣布暂停使用CRISPR / Cas9以可遗传的方式编辑人类基因组(尽管有迹象表明研究人员已经打破了这一禁令)。他们说,他们对这个过程以及这样做的长期影响知之甚少。但像刘的研究有朝一日可以在微调这些工具并使其适合人类使用方面发挥作用。
“我们正在努力了解基因组编辑酶的机制,这种机制可能对未来的制药和治疗应用具有巨大潜力,这可能使我们更接近这种技术可用于人类疾病的位置,”刘说“没有TACC资源这项研究是不可能完成的。“
推荐内容
-
八角亭迷雾念玫和谁睡过到底是谁的孩子?玄梁究竟有几个妹妹叫什
Hello,大家好!今天的你们都开心了吗?都在忙些什么呢?今天小编要和大家一起聊聊近期热播的电视剧八角亭迷雾玄梁有几个妹妹跟谁睡了一事。下
-
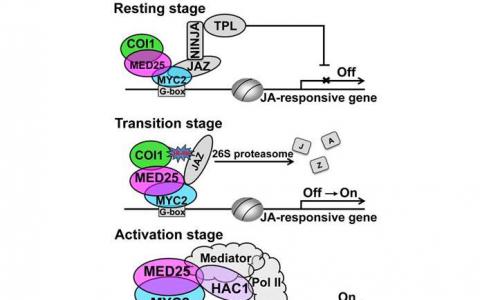
研究阐明了植物中的核激素受体功能
植物使其生长和发育适应不断变化的环境的惊人能力是由多种植物激素调节的,这些激素几乎调节植物生命的各个方面。在过去的10到15年中,在阐
-
9月2日扬州蜀冈-瘦西湖风景名胜区疫情最新数据公布 昨日扬州
提醒:疫情未结束,防范措施不可松懈。勤洗手。使用肥皂或洗手液并用流动水洗手,用一次性纸巾或干净毛巾擦手。双手接触呼吸道分泌物后(如
-
微针丸可用于口服胰岛素剂量
来自美国,丹麦和瑞典的一个国际研究团队开创了一种新方法,该方法可以吞咽胰岛素,而不是向临床注入更近一步。科学家们开发了一种可摄...
-
维生素D与提高野生动物的生育能力有关
一项对野羊的研究发现,高水平的维生素D与提高生育能力和繁殖成功率有关。这项研究在偏远的赫布里底群岛进行,增加了越来越多的证据表明维
-
11月27日石家庄疫情最新数据公布 石家庄昨日有1例确诊病例治
温馨提示:尚未接种新冠病毒疫苗的群众(有接种禁忌症除外),请尽快持本人身份证到附近的接种点完成疫苗接种。继续加强个人防护意识,养...
-
8月7日郑州市疫情最新数据公布 郑州现有确诊病例18例详情(截
郑州现有确诊病例18例,无症状感染者100例。那么,对于郑州疫情的这个话题,今天的你是否也在关注着?具体什么情况?下面跟小编一起来了解下
-
传闻中的陈芊芊结局 陈芊芊为救韩烁而死
近日由赵露思主演的电视剧传闻中的陈芊芊热播相信不少剧迷对于剧中的结局也是充满了好奇,那么传闻中的陈芊芊结局是什么呢?最近一部《传闻
-
虎牙大象是什么意思什么梗?虎牙只有一个大象那就是大象是什么意
今天小编为大家带来一则关于虎牙大象是什么梗最新文章,如果觉得本篇文章对你来说有帮助的话,别忘了点赞、评论、转发和收藏哦!该梗出自虎
-
2021花呗新规定是什么?2021年花呗全面关闭吗?
想必大家都知道,蚂蚁花呗是蚂蚁金服推出的消费信贷产品,花呗的用户被授信透支额度。开通成功后,消费者本月花,下月付,按时还款还不...