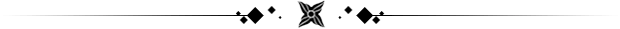研究为A组链球菌提供了新的见解
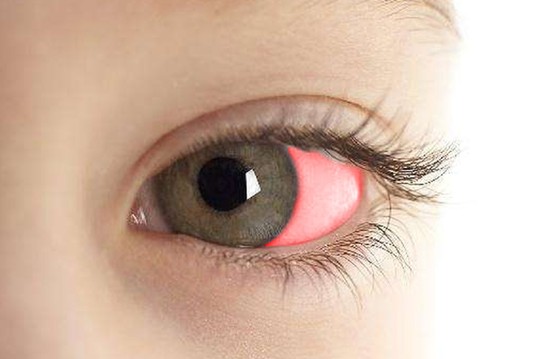
一种细菌病原体导致一系列疾病,从咽炎和脓疱病到更严重的诊断,如中毒性休克综合征和坏死性筋膜炎(肉食性疾病),一种严重的细菌性皮肤感染,迅速传播并杀死身体的软组织。该病原体被称为A组链球菌,仍然是全球性的健康负担,每年报告的病例估计有7亿,并且由于严重感染导致超过50万人死亡。
一个多世纪以来,观察到A组链球菌(GAS)诱导红细胞快速破坏的能力,并且仍然是GAS诊断的临床标志。这种破坏是由于被称为链球菌溶血素S(SLS)的 GAS产生小肽毒素。虽然人们普遍认为SLS通过膜破坏发挥其裂解活性 - 红细胞的过度破坏,但其确切的作用方式仍然未知。
“我们实验室和其他人最近进行的分子研究表明,SLS是一种肽毒素,与一类被称为细菌素的细菌产生的化合物有关,”圣母大学生物科学副教授Shaun Lee说。“许多这些相关的细菌素已经定义了细胞靶标,并且未被证明可以作为细胞膜的一般溶解剂起作用。”
在一项新的研究中,Lee的研究小组提供了第一个实时,高分辨率的A组链球菌红细胞破坏观察,也称为β-溶血。
“我们证明SLS长期观察到的红细胞溶血不是由于红细胞膜的一般性破坏引起的,正如之前所认为的那样,而是该作用是由于SLS毒素直接靶向的能力红细胞表面特定的外膜蛋白,主要红细胞阴离子交换蛋白带3“。
重要的是,Band 3功能的化学抑制完全阻断了SLS的溶血活性,并显着改变了GAS在体内皮肤感染模型中诱导的病理学。“我们的研究为长期存在的SLS功能问题提供了第一次机械研究,重要的是,开辟了治疗严重GAS疾病的新治疗途径,”Lee说。
“这是我实验室的高级研究员Dustin Higashi领导的一次精彩的合作努力,旨在回答这个长期存在的神秘感,这种毒素被称为Streptolysin S,溶解红细胞,导致该组织引起的侵袭性人类疾病。一种链球菌,“他说。
在弗朗西斯卡斯特利诺和维多利亚普罗普利斯的指导下,在WM凯克转基因研究中心进行的体内研究提供了对支持我们假设至关重要的研究结果。使用人源化小鼠模型,凯克科学家Deborah Donahue和Jeff Mayfield证明了在GAS感染期间阻断SLS毒素的作用,感染部位的病理学可能会大大减少。这些发现具有开发治疗由A组链球菌引起的严重疾病的新疗法的巨大潜力。
推荐内容
-
心理知识:偷走幸福的消极心理_偷走幸福有何消极心理
随着社会压力的不断加大,人们现在把越来越多的目光放到了一个人的心理情况上。确实,每个人的抗压指数是有限的,一个平时看着正常的人...
-
炒作“大陆威胁”者才是台海和平的真正威胁
炒作“大陆威胁”者才是台海和平的真正威胁 作者 | 王平 继民进党当局给岛内民众发放所谓“全民防务手册”后,有美国政客又扬言将...
-
研究人员使用TACC超级计算机揭示黄冠综合症的遗传根源
自2011年以来,一种被称为黄冠病综合症(YCS)的神秘疾病折磨着澳大利亚的甘蔗。这种情况导致其他健康植物的中冠叶片迅速变黄,达到植物糖产
-
食盐中的亚铁氰化钾有毒吗?真是如此?
随着互联网的快速发展,我们在获取信息的时候很容易被带跑方向。有时候真相也许并不是网上说的那样,所以我们必须要有自己的判断和独立...
-
每天喝两口,有益健康?看看真相是什么
生活中我们经常会听见各种各样的流言,但是只要我们用心去思考和辨认其实 不难发现这些谣言有很多破绽。所以今天,小编照常给大家辟谣一则
-
心理知识:固执心理形成的原因
心理这个词最近被提及的频率是越来越高了。其实在国外有一个职业特别吃香,那就是心理医生。为什么呢?因为国外特别是西方有几个国家已...
-
眼白一片鲜红就是眼底出血吗?大家都来看看
互联网时代,每个人都是信息传播者,但是我们必须清楚一点:在没有获得真正证实的消息之前,千万不能随意散播谣言,很容易造成以讹传讹...
-
常吃黑豆难补血,科学数据来解答?很多人想问
日常生活中我们经常会听到各种各样的坊间流言。然而很少人去求证这些流言的真实性,久而久之就变成了真事。在这里,小编必须提醒大家,...
-
心理知识:自恋狂的十大标志 你的身边有吗?
生活中,不管我们在跟自己独处还是跟别人相处的过程中其实我们会发现心理对一个人的影响是很大的。因此当我们发现自己有心理疾病的倾向...
-
抑郁焦虑情绪如何缓解以及注意事项
心理这个词最近被提及的频率是越来越高了。其实在国外有一个职业特别吃香,那就是心理医生。为什么呢?因为国外特别是西方有几个国家已...