细胞内三维运输
路德维希马克西米利安大学的研究人员已经将蛋白质合成,运输和修饰之间复杂的相互作用可视化。
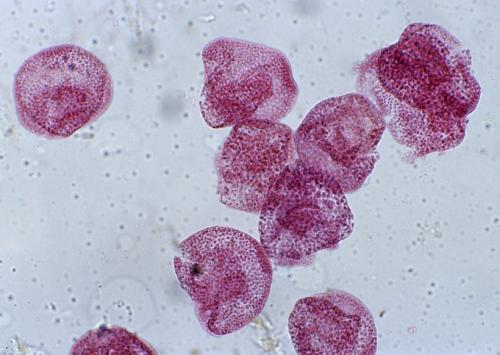
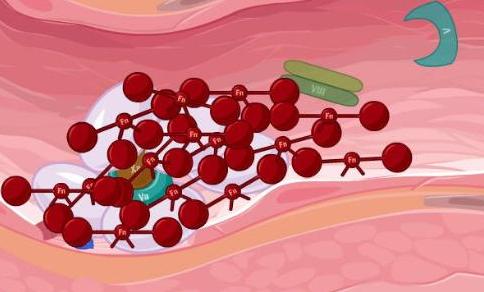
高等生物的细胞被称为内质网(ER)的管状网络密集地填充。ER驻留复合物作为核糖体的结合平台,核糖体是负责蛋白质合成的细胞机器。ER附着的核糖体合成用于各种细胞内和细胞外位置的蛋白质。为了保证成功递送,许多这些蛋白质在通过ER膜时用地址标签的分子当量进行化学修饰。由基因中心的Roland Beckmann教授领导的LMU研究人员与马克斯普朗克生物化学研究所的同事合作,现已确定了大分子复合物的三维结构,该结构将该标记步骤与核糖体蛋白质合成和蛋白质转运相结合。 ER膜。他们的研究为详细了解这一重要的细胞过程提供了基础,并已发表在“科学”杂志上。
所有生物膜都由磷脂双层组成,其对极性(带电荷)分子如蛋白质基本上是不可渗透的。然而,某些特殊蛋白质可以作为其他蛋白质通过脂质双层通道的通道。在ER膜上,这种“易位子”允许由ER结合的核糖体合成的蛋白质分别进入ER内部或整合到ER膜中。当它穿过膜时,通过在称为糖基化的过程中附着由14个糖分子链组成的“寡糖”,在特定位点修饰生长的蛋白质。这种化学标签确保蛋白质随后被送到正确的目的地。此外,该标签在使新生蛋白质折叠成其生物功能所需的适当形状方面起着至关重要的作用。“糖基化错误导致不正确折叠的蛋白质积累,而这些蛋白质反过来激活细胞应激反应- 通常会给细胞带来致命的后果,“Beckmann团队的成员,新研究的第一作者Katharina Braunger说。
附着作为新生蛋白质链的寡糖的酶复合物通过核糖体通过易位子进料,称为OST(寡糖基转移酶)复合物。在高等生物中,OST复合物存在于两种不同的组合物中。Beckmann及其同事利用低温电子显微镜和图像的组合,现已获得结构证据,证明这两种形式的功能也不同。A型OST与活性核糖体和蛋白质传导通道相互作用形成稳定的复合物,并改变生长的蛋白质在生产过程中。相反,另一种变体不能与易位子结合。“B变种负责证明阅读以及A变体无法访问的网站的修改,”Beckmann说。新数据使团队能够确定核糖体结合OST复合物中亚基的三维组织,并开发其功能的分子模型。该模型允许他们提出两种变体之间特异性差异的基础,并解释蛋白质转运和糖基化如何机械耦合。
推荐内容
-
生物学家追踪有助于培养结核病多重耐药性的基因
科学家对超过6,000种结核分枝杆菌临床分离株进行了基因测序,这是一种致病性结核病(TB),一种通常会攻击肺部的空气传播疾病。在努力确定导
-
保护基因组研究中的机密性
全基因组关联研究寻找特定遗传变异与疾病发病率之间的联系,是许多现代生物医学研究的基础。但基因组信息数据库会带来隐私风险。从人们...
-
血友病是一种遗传疾病 预防的重要措施就是产前基因检测
血友病患者又被称为玻璃人,因为一旦患上血友病那么患者凝血功能就会出现障碍,稍有不慎就血流不止。4月17日是世界血友病日,昨天,记者获
-
用于评估干细胞发育的新生物标志物
由UCL科学家领导的一个研究小组已经找到了一种方法来评估被称为诱导多能干细胞(iPSCs)的制造干细胞的可行性。今天在Nature Communications
-
新型纳米载体可以为健康细胞提供更高效 更低毒性的传递
来自埃及和沙特阿拉伯的研究人员设计并合成了新的有机聚合物,作为有效的药物纳米输送系统具有很大前景。许多药物,特别是用于治疗癌症...
-
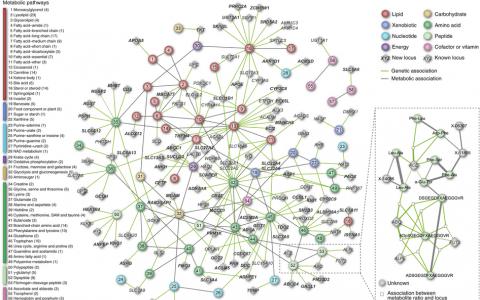
新陈代谢的遗传图谱
一个国际财团已经制作了一个影响人体新陈代谢的基因综合图谱,并确定了共同控制关键代谢物血液浓度的变体。上个月在Nature Genetics1上发
-
常用的统计方法是缺少DNA变异与疾病之间的关联
各种统计学方法被用于研究DNA构成和特定疾病的微小变化之间的关联。研究人员验证了一种产生更多结果的统计方法1。国际研究团队,包括隶属于
-
微生物的全球运输
一系列国际研究人员,包括麦格理大学的Michael Gillings教授认为,废水,旅游和贸易正在以前所未有的规模推动全球各地的微生物传播。这篇
-
新的基因工程技术可以帮助设计 研究生物系统
一项新技术将帮助生物学家修补基因,无论目标是将细胞转变为生产药物的小工厂,修改作物以在有限的水中生长,还是研究基因对人类健康的...
-
干细胞将自己组织成假胚胎
哺乳动物体的确定结构在胚胎植入子宫后不久建立。身体的前后,腹侧和中侧 - 外侧轴在基因网络的控制下组织起来,所述基因网络协调胚胎各