细胞代谢调节致病性T细胞与调节性T细胞之间的命运决定
患有自身免疫性疾病(例如多发性硬化症,炎症性肠病和类风湿关节炎)的患者在两种类型的免疫系统T细胞之间存在失衡。介导慢性炎症的破坏性Th17细胞升高,抑制炎症反应并在自身免疫性疾病中起保护作用的调节性T细胞或Treg细胞减少。

两种细胞都与相同的前体-幼稚的CD4 T细胞-区别开来,它们转变为Th17或Treg细胞的开始都是从相同的信号开始的。随后,命运的决定发生了,就像路上的叉子一样,引导变化中的CD4细胞成为炎症性T细胞或调节性T细胞。
由阿拉巴马大学伯明翰分校UAB细胞,发育和整合生物学系副教授Laurie Harrington博士领导的新的临床前研究表明,细胞代谢在调节这一命运决定中起着关键作用。决定在CD4 T细胞活化的早期发生。这为操纵T细胞的细胞代谢提供了一种新的,有希望的治疗干预手段,以调节慢性自身免疫性疾病中致病性Th17细胞与Treg细胞之间的平衡,这是一个可能性。这项研究发表在《细胞报告》杂志上。
激活后,已知T细胞会迅速增加新陈代谢,包括糖酵解和线粒体氧化磷酸化或OXPHOS,以满足分化的能量需求。但是还没有确定OXPHOS对Th17分化的确切贡献。
UAB研究人员和纽约大学的一位同事发现,Th17分化过程中ATP连接的线粒体呼吸对于上调糖酵解和TCA循环代谢至关重要。令人惊讶的是,如多发性硬化症的小鼠模型所示,通过Th17促进中枢神经系统的炎症也很重要。
在小鼠模型中,实验性自身免疫性脑炎,Th17细胞引起疾病进展。对于实验,使用Th17极化细胞因子的组合来分化收获的CD4 T细胞。一组是极化的对照,一组在存在线粒体OXPHOS抑制剂的寡霉素的情况下极化。然后将T细胞转移到实验小鼠中。在极化条件下接受用寡霉素处理过的T细胞的小鼠显示出明显的疾病发作延迟和疾病严重程度降低。两组T细胞在转移后均强烈增殖。
在机械实验中,研究人员详细介绍了在存在或不存在寡霉素的情况下极化的细胞之间不同的早期分子事件。这些包括上调或下调的基因集,Th17或Treg细胞标记物的存在与否,Th17分化所需的签名转录因子的表达以及在T细胞受体信号传导中起作用的基因产物的表达。
命运决定的时机出乎意料。在一项实验中,仅在最初的24小时内,将CD4 T细胞暴露于Th17极化条件下,同时存在寡霉素。然后洗涤它们,并使其在偏振条件下继续分化。短暂暴露于寡霉素的影响是缺少Th17标记的T细胞,而是显示Treg细胞的标志,包括Foxp3的表达。因此,短暂的早期暴露于寡霉素影响了Foxp3的命运决定。
总的来说,Harrington说:“线粒体OXPHOS的抑制作用在多发性硬化小鼠模型中消除了Th17的致病性,并导致在Th17条件下产生功能抑制性Treg 细胞。”
推荐内容
-
研究有助于开发具有抗菌特性的新药
该研究在CEU UCH进行,将分子类型学和QSAR方法结合起来作为更快,更实惠的工具,以获得新药并挑战不断增长的细菌耐药性。由于在人类和动物
-
肝病医生胡远忠:乙肝大三阳该如何治?
肝病医生胡远忠:乙肝大三阳该如何治? 原标题:肝病医生胡远忠:乙肝大三阳该如何治?
-
土壤中的细菌多样性受冰河时代的影响
从药物的角度来看,很少有微生物像链霉菌一样有价值:这一类细菌是目前使用的80%抗生素的来源。一项关于其在北美土壤中分布的新研究表明,
-
只要妈妈在,孩子就不乖?背后藏着你不知道的婴幼儿心理学
只要妈妈在,孩子就不乖?背后藏着你不知道的婴幼儿心理学 原标题:只要妈妈在,孩子就不乖?背后藏着你不
-
苏州:发现高速路废弃物部分样本为阳性
苏州:发现高速路废弃物部分样本为阳性 原标题:苏州:发现高速路废弃物部分样本为阳性
-
喙鲸可能经常被标记为采矿的海底斑点
鲸鱼可能在未来深海采矿的太平洋部分地区的海底上留下了痕迹。研究人员8月22日在英国皇家学会开放科学杂志上报告说,在海底雕刻的成千上万
-
基因测试旨在改善赛马的表现
总部位于UCD的马科学公司Plusvital推出了四项新的基因测试,旨在使纯种马达到完整的赛马和繁殖潜力。该公司的新基因测试可以为纯种马主和育
-
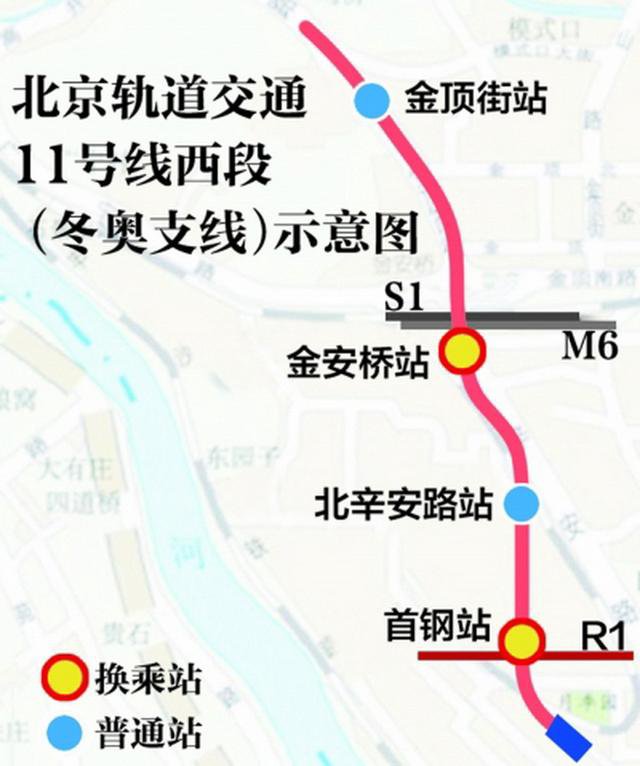
北京地铁11号线最新消息 附北京11号线全程线路图一览
想必大家都知道,北京地铁11号线,是中国北京市正在建设的一条地铁线路。那么,你知道北京地铁11号线什么时候开通吗?北京地铁11号线西段最
-
河南通报幼师发亲吻男童视频事件 责令幼儿园停业整顿
河南通报幼师发亲吻男童视频事件 昨天一则关于河南幼师发亲吻男童视频事件持续发酵中,随着该事件的发展,今天最新进展来了。事情发...
-
11月18日上饶市疫情最新消息公布 上饶市发热门诊、红黄码人
上饶市发热门诊、红黄码人员医疗救治定点医疗机构公布。据消息显示,各县(市、区)、上饶经济开发区、三清山风景名胜区、上饶高铁经济试...