呼吸道合胞病毒疫苗进入临床试验
在马里兰州贝塞斯达的国立卫生研究院临床中心开始进行一项临床试验,以测试呼吸道合胞病毒(RSV)研究疫苗的安全性和耐受性。该试验还将评估疫苗在健康成人参与者中促进免疫反应的能力。该研究疫苗由美国国立卫生研究院国家过敏和传染病研究所(NIAID)的科学家开发。
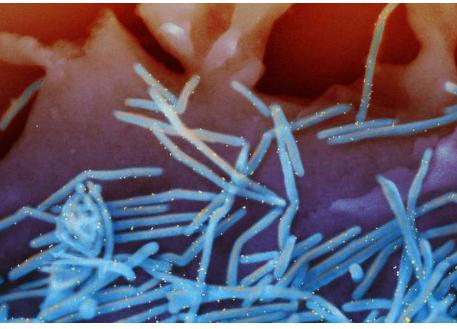
大多数人在2岁时感染RSV,并且在整个生命过程中经历反复感染。受感染的成人和儿童通常会出现轻微的感冒症状,并在一到两周内消退。然而,感染可导致严重的下呼吸道疾病,包括肺炎和细支气管炎,早产儿,2岁以下有心脏或肺部问题的儿童,免疫系统较弱的儿童和成人以及老年人。大约2%的1岁以下RSV感染婴儿需要住院治疗。1至5岁的儿童和65岁以上的成年人住院的风险也较高。
在美国,RSV每年平均导致5727例住院治疗,并且在5岁以下儿童中接受210万次门诊治疗; 根据美国疾病控制和预防中心的数据,65岁以上的成年人中有177,000人住院,14,000人死亡。在全球范围内,RSV感染估计每年导致超过250,000例死亡。
目前没有可用于预防RSV感染或药物治疗的疫苗。单克隆抗体帕利珠单抗在美国被许可用于预防高风险儿童中由RSV引起的严重下呼吸道疾病,但它不被许可用于一般人群。
“RSV被认为是导致疾病和死亡的主要原因,不仅在婴儿和儿童中,而且在免疫系统和老年人减弱的人群中也是如此,”NIAID主任Anthony S. Fauci医学博士说道,“减轻这种负担的疫苗”非常需要重要的疾病。“
这项名为VRC 317的研究将招募年龄在18-50岁的健康成年人。参与者将被随机分配,在12周内接受两次注射,使用研究性疫苗或用明矾佐剂化的研究性疫苗。明矾是一种常用于疫苗的化合物,可增强人体的免疫反应。
参与者还将被随机分配接种疫苗接种时间点的三种疫苗剂量(50微克,150微克或500微克)中的一种。最初,五人将接种50微克剂量的疫苗。如果最初的参与者组没有经历由疫苗引起的严重不良反应,则研究小组将开始在下一剂量水平为接种者接种疫苗。他们将重复这个逐步的过程,直到他们施用500微克剂量。
第一次注射后,参与者将在44周内返回12次就诊。在这些访问中,研究临床医生将进行体检并收集血液样本。他们还将测试志愿者口腔和鼻子的粘液样本,以测量产生的免疫反应。
该研究由首席研究员Michelle C. Crank博士领导,他是NIAID疫苗研究中心(VRC)病毒发病实验室部分转化科学核心负责人。研究临床医生将对任何新的临床信息进行日常安全性审查,协议安全审查小组将每周检查试验安全性数据,以确保疫苗符合安全标准。
这种名为DS-Cav1的研究性疫苗来自多年的研究,该研究由临时VRC主任Barney S. Graham博士和结构生物学部主任Peter D. Kwong博士领导。 VRC的结构生物信息学核心。该候选疫苗是单一的,结构工程从RSV,而不是基于弱化或灭活的全病毒更传统方法的表面蛋白。2013年,VRC科学家在小鼠和非人灵长类动物中测试了几种版本的蛋白质作为疫苗。蛋白质变体引发高水平的中和抗体并保护动物免受RSV感染。博士。格雷厄姆和邝选择最有希望的候选人DS-Cav1进行临床评估。
格雷厄姆博士说:“这项工作代表了一个例子,说明基础研究的新生物学见解如何能够为具有公共卫生重要性的疾病提供候选疫苗,以及多学科研究团队的价值,例如在VRC组装的研究团队。”
推荐内容
-
教你川味水煮鱼的做法,麻辣鲜香,开胃下饭,跟饭店的味道有一拼
教你川味水煮鱼的做法,麻辣鲜香,开胃下饭,跟饭店的味道有一拼 原标题:教你川味水煮鱼的做法,麻辣鲜香
-
整形手术后新加坡女性获得信心
自从她还是一个年轻女孩以来,她一直因为饱满而被戏弄,导致她在八年内减掉超过20公斤。经过多年的节食,服用减肥药,运动和体重波动,...
-
尿酸500是肾有问题吗?高尿酸如何清除?
尿酸500是肾有问题吗?高尿酸如何清除? 原标题:尿酸500是肾有问题吗?高尿酸如何清除?
-
腹黑金毛经常坑来来,结果来来是饿了一天
腹黑金毛经常坑来来,结果来来是饿了一天 原标题:腹黑金毛经常坑来来,结果来来是饿了一天
-
留学生都是怎么度过最开始的困难期 留学生必备技能
很多留学生到了一个陌生的环境,都会难以适从,毕竟是语言、生活习惯、饮食等的全方面改变,那么还是看看前人都是怎么习惯的吧。人确实...
-
外卖小哥16秒停住失控汽车 不是在送外卖就是在拯救世界
有一句话是,外卖小哥不是在送外卖的路上,就是在拯救世界的路上。这一次,视频为证!近日,新疆乌鲁木齐,一辆红色轿车因未拉手刹在马路中
-
8月6河南安阳疫情最新实时数据消息公布 安阳昨日发现1例新冠无症
河南安阳发现1例新冠病毒无症状感染者,活动轨迹公布。那么,对于安阳疫情的这个话题,今天的你是否也在关注着?具体什么情况?下面跟小编一
-
科学家们揭示了DNA的三维排列如何帮助物种长期存在
从父亲到儿童,遗传信息的传递需要在精子中仔细包装DNA。但是,自然包装这种DNA以备后代的方式尚不清楚。科学家利用新技术揭示成熟雄性生殖
-
四川发现褪色小熊猫是什么情况?网友:“罕见SSR小熊猫”
【导读】说起小熊猫,想必大家都知道,它是小熊猫科小熊猫属的一种动物。外形像猫,但较猫肥大,全身红褐色。于2013年CNN评选的世界最可爱
-
苏州市疫情防控2022年第133号通告
苏州市疫情防控2022年第133号通告 原标题:苏州市疫情防控2022年第133号通告