中胚层FDA同意通过BLA治疗心力衰竭细胞疗法
Mesoblast今天表示,它和FDA已经就植入左心室辅助装置(LVAD)的终末期心力衰竭患者的公司同种异体细胞治疗产品候选Revascor的营销应用达成了临床路径。

该途径将包括对LVAD患者的Revascor验证III期试验,其结果将成为BLA申请的基础。Mesoblast说,确证试验的主要终点是主要粘膜出血事件的减少,而关键的次要终点将包括证明心血管功能各种参数的改善。
根据今年早些时候签署的谅解备忘录,计划在纽约西奈山伊坎医学院与国际健康成果和创新研究中心(InCHOIR)一起进行验证性试验。
“我们将与FDA和InCHOIR密切合作,以生成Revascor全面上市批准所需的确认临床数据,以预防LVAD植入物在终末期心力衰竭患者中的这种威胁生命的炎症并发症,”Mesoblast首席执行官Silviu Itescu,MBBS,FRACP在一份声明中说。
Itescu最近在接受GEN采访时说,该机构在7月份的会议上给了Mesoblast“Revascor非常积极的反馈”。一个月前,FDA已批准Revascor的一种孤儿药指定用于预防植入后粘膜出血,包括来自胃肠(GI)道,需要LVAD的终末期慢性心力衰竭(CHF)患者。
在2018年美国心脏协会科学会议上,NIH心胸外科试验网络研究人员介绍了Revascor 的159例患者,安慰剂对照IIb期研究(NCT02362646)在终末期心力衰竭中的结果。
胃肠道出血减少76%
结果显示,单个心肌内剂量的细胞疗法候选物导致主要胃肠道出血事件减少76%,并且植入LVAD的终末期心力衰竭患者的相关住院减少65%。美国食品和药物管理局已同意Mesoblast认为,出血减少是植入LVAD患者的重要临床结果,该公司援引研究表明,多达40%的患者因主要胃肠道出血而再次入院。
结果还显示,与对照组相比,Revascor在6个月时没有达到统计学上显着的LVAD支持暂时断奶(61%对58%),结果Mesoblast说反映了血液凝块。IIb期试验由NIH国家心脏,肺和血液研究所(NHLBI)和加拿大卫生研究院资助和赞助。
美国食品和药物管理局已向该公司证实,IIb期试验的数据可以通过BLA支持产品上市许可以及确认的临床数据,Mesoblast说。
Revascor-曾被称为MPC-150-IM和rexlemestrocel-L-由1.5亿个间充质前体细胞(MPC)组成,通过直接注射到患有CHF和心功能进行性丧失的患者的心肌中。
“我们相信,通过关闭炎症过程,我们的细胞能够充分逆转异常脉管系统,从而减少出血,”Itescu说。
Revascor是FDA的再生医学高级疗法指定,通过创建21所管制ST世纪治愈法加速用于治疗严重疾病和生命危险的细胞疗法的发展。
Revascor也是另一项III期试验(DREAM HF-1,NCT02032004)的主题,旨在评估晚期心力衰竭的候选人。该试验已完成北美55个中心的患者入组,566名患者随机接受Revascor或安慰剂。Mesoblast今年早些时候表示,这项研究将在已经产生足够的主要终点事件时完成。
推荐内容
-
8月4日海南疫情最新实时消息公布 海南昨日发布在琼人员非必
【导读】坚持常态化疫情防控措施。在商场、餐厅、酒店、影剧院、体育场等公共场所,积极配合戴口罩、验码测温、一米线等措施。乘坐公共...
-
研究发现蔓越莓在减少老年妇女尿路感染方面缺乏益处
在居住在疗养院中的老年妇女中,与安慰剂相比,蔓越莓胶囊的施用导致细菌尿和脓尿的存在(尿液中细菌和白细胞的存在,尿路感染[UTI]的迹象)
-
俄罗斯一男子全身倒扣死在雪地脸部被埋 遗体下物品让人毛骨悚然
居民发一名现男子跪倒雪地一动不动,还将脸部埋进了雪地里,旁边还有一瓶白兰地。那么,真相是什么呢?今天的你是否在关注男子全身倒扣死在雪
-
吉娜德国版鸡打鸣是什么梗?吉娜个人资料简介
《王牌对王牌收官》,嘉宾请来了朗朗吉娜夫妻等明星,在昨日的节目中沈腾为郎朗娇妻吉娜起中文名吉凤芝,引发了网友热议。具体是怎么回...
-
地球的河流覆盖的土地比我们想象的多44%
与美国德克萨斯州相比,世界上所有的河流和溪流都覆盖了更多的区域。根据全球卫星图像的新估计显示,这些水道在约773,000平方公里的土地上
-
准新郎路上丢10万元彩礼是怎么回事?10万彩礼多吗?
结婚彩礼是中国从古至今婚嫁流传下来的习俗,是男方给予女方的聘礼,因此在男女双方结婚时就要送上彩礼。可近日却发生了一起准新郎路上丢10
-
四川一村民山坡上偶遇“国宝”大熊猫兴奋不已 随后脱口而出大
四川村民偶遇野生大熊猫兴奋不已,脱口而出的大哥一词引发爆笑一幕。今天的你,是否在关注这个话题呢?针对此消息,小编收集了一些相关的...
-
今日山东滨州疫情最新数据情况 山东滨州新增“1+3”境外输入病例
【导读】小编在这里提醒大家,我们目前取得的成果来之不易,跟病毒的斗争可能会是长期的持久战,不能自以为战胜了病毒就放松自己,为了...
-
为什么掰指关节会这么吵
砰的一声响了起来——但为什么呢?科学家们对于为什么掰指关节会发出噪音意见不一。现在,一种新的数学解释表明声音是由于关节液体中微小...
-
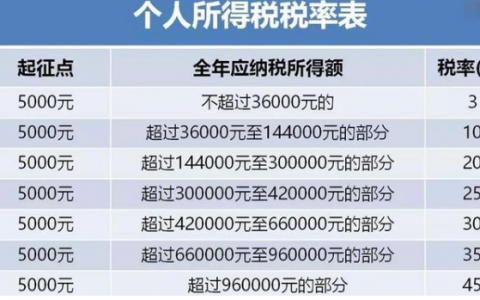
工资5000块要扣多少个人税?什么是个人税?
缴纳个税是每个公民的义务,那么新个税法实施之后,工资5000以上扣多少税呢?缴纳个税的比例又是怎样算呢?下面一起来了解下。个人所得税与企业