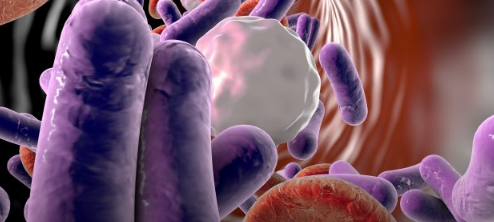
抗癌药物有望治疗人类乳头瘤病毒
阿拉巴马大学伯明翰分校(UAB)的科学家报告说,癌症药物vorinostat、belinostat和panobinostat可能被重新用于治疗由人类乳头瘤病毒(HPVs)引起的感染。
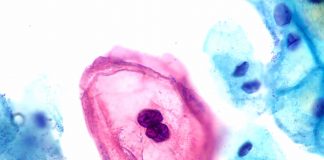
目前存在针对HPV感染的高效疫苗,包括最近批准的Gardasil 9,该疫苗对已知的9种可导致宫颈癌、外阴癌、阴道癌和肛门癌以及生殖器疣的HPV基因型进行免疫。但是这种疫苗需要在人变得性活跃之前接种,因为它对现有的HPV感染没有治疗效果。
UAB生物化学和分子遗传学助理教授、vorinostat研究(“vorinostat,一种泛hdac抑制剂,可消除HPV-18的DNA扩增”)的主要作者N. Sanjib Banerjee博士说:“目前迫切需要安全、有效和廉价的治疗药物。”
UAB的Louise Chow博士和Thomas Broker博士的实验室发现,HPV感染的发展依赖于上皮细胞向全层鳞状上皮细胞的分化。此外,HPV在这些分化细胞中重新激活宿主DNA复制,使复制蛋白和底物可用于支持病毒DNA扩增。
hpv引起上皮细胞增生疾病。高危基因型对黏膜上皮细胞的持续感染可发展为高度发育不良和癌症。病毒转录和蛋白活性与组蛋白乙酰转移酶和组蛋白去乙酰化酶(HDACs)的调控密切相关,这两种酶能重塑染色质并调节基因表达。HDACs对于重新建模和修复复制染色质也至关重要,以支持复制叉的进展。因此,vorinostat (suberoylanilide hydroximic acid)和其他泛hdac抑制剂被用于治疗淋巴瘤,”研究人员写道
在这里,我们研究了vorinostat对人角质形成细胞有机类型培养中高危HPV-18的生产性感染的影响。HPV DNA在鳞状上皮细胞有丝分裂后的分化细胞中扩增,其中病毒的癌蛋白E7和E6通过破坏主要的肿瘤抑制因子pRB家族蛋白和p53的稳定,建立了一个宽容的环境。我们发现vorinostat显著降低了这些E6和E7活性,消除了病毒DNA扩增,抑制了宿主DNA复制。e7诱导的DNA损伤反应对这两个事件都至关重要,但也受到了损害。因此,vorinostat暴露可导致hpv感染的分化细胞DNA损伤并引起细胞凋亡,而未感染的组织则得以幸免。细胞凋亡是由于高水平的促凋亡Bim亚型,已知EZH2在含有HDACs的抑制因子复合物中抑制了该亚型。另外两种HDAC抑制剂belinostat和panobinostat也能抑制病毒DNA扩增并引起细胞凋亡。我们认为HDAC抑制剂是很有前途的治疗药物,可以治疗良性HPV感染,消灭子代病毒生产,从而阻断传播。
Chow和Broker实验室通过在空气介质间期(air-media interphase)培养原代人角质形成细胞两到三周,再造了一个完全分化的人类鳞状上皮细胞,他们称这种生长为raft培养。2009年,他们的实验室开发了一种HPV-18感染的原始人类角质形成细胞筏式培养模型,允许HPV-18 DNA的强劲扩增和感染性病毒后代的产生。这种多产的筏培养是潜在抗hpv药物临床前研究的理想模型。
Banerjee博士和他的同事们假设HDACs的抑制剂会抑制HPV DNA扩增,因为它们已知的机制是干扰染色体DNA复制。染色体复制需要组蛋白的HDAC改变。Vorinostat抑制了许多HDACs,因此它不仅可能中断染色体复制,还可能中断病毒DNA复制。
使用HPV-18模型raft培养,研究人员发现vorinostat可以有效抑制HPV-18 DNA的扩增和病毒的产生。重要的是,vorinostat也能诱导部分分化细胞凋亡。当染色体DNA复制中断时,细胞死亡可归因于DNA断裂。另外两种HDAC抑制剂belinostat和panobinostat也获得了类似的结果。相比之下,未受感染的筏式培养的未复制DNA的分化细胞,在有抑制剂的情况下,大部分得以存活。
UAB团队还研究了vorinostat如何影响病毒癌蛋白的水平和功能,并描述了在hpv -18感染的培养基中导致程序性细胞死亡的机制。“在这些详细研究的基础上,”班纳吉博士说,“我们认为,HDAC抑制剂是治疗良性HPV感染的有希望的化合物,它能抑制子代的产生,从而阻断感染传播。”
UAB小组还报告说,vorinostat在含有HPV-16的增殖不良和癌症细胞系的筏式培养中导致大量细胞死亡。HPV-16和HPV-18是导致肛门和口咽部癌症的最普遍、高危的hpv。Banerjee博士说:“但是还需要进一步的研究来验证这些制剂在治疗HPV相关的异常增生和癌症方面是否有用。”
推荐内容
-
坐月子不能洗头吗?
坐月子不能洗头吗? 原标题:坐月子不能洗头吗?
-
今日东莞麻涌疫情最新数据公布 东莞通报19岁确诊大学生感染来
大家都知道上一年疫情已经快要结束了,谁也没想到今年又有多地出现疫情,如广东。那么,你知道当前疫情究竟是什么情况吗?下面跟小编一起来了
-
今日上海疫情最新消息 张文宏深夜发文要重视了!
新冠的出现是逆全球化的最好机会,各国采取严格的出入境政策和更加严格的检验检疫手段,势必会阻碍全球化。但是,疫情在一定程度上不但...
-
刚刚,上海通报:明天起分阶段推进复商复市!昨日本土新增“166+1
刚刚,上海通报:明天起分阶段推进复商复市!昨日本土新增“166+1203”,108岁高龄的重症患者已出院 原标
-
大型动物器官串扰研究为败血症提供了新的思路
研究人员在一个大型败血症动物模型中研究了受影响器官之间的代谢变化,他们说,他们已经确定了潜在的常见和器官特异性代谢变化,这些变...
-
研究人员发现了自发形成的半导体纳米管
如果科学家能够找到一种方法来控制纳米尺度制造半导体元件的过程,他们就可以为这些元件提供独特的电子和光学特性 - 为大量有用的应用打
-
江西戴亚利犯了什么事会坐牢吗?戴亚利个人资料将面临什么刑罚
想必这两天,大家对于戴亚利是谁怎么了一事是非常关注的,具体是什么情况呢?下面跟小编一起来了解下事件始末。据消息显示,戴亚利,江西省
-
五名研究人员分享了50万美元的基因编辑工作奖
五名研究人员将分享一项价值50万美元的医疗奖,因为他们在开发一种突破性的基因编辑工具中可以让科学家改变活细胞的DNA。周二宣布了奥尔巴
-
最新消息:美国罗斯福号航母840人确诊
美国罗斯福号航母840人确诊是真的吗?今天一则关于美国罗斯福号航母840人确诊的消息登上了热搜,想必大家对于美国罗斯福号确诊一事是非常感
-
霍尊的小琵琶精是谁被扒出来了?霍尊的小琵琶精是施冰岚吗都有谁
一起吃瓜,一起八卦,一起畅游娱乐圈,最近一段时间你是否有关注娱乐圈的热门事迹呢?下面跟小编一起来啃啃今日份的大瓜吧!霍尊的小琵琶精是谁