合理应用喹诺酮类抗茵药物治疗下呼吸道感染专家共识
-
合理应用喹诺酮类抗茵药物治疗下呼吸道感染专家共识
中华医学会呼吸病学分会感染学组
一、喹诺酮类抗菌药物的发展历程[1-5]
喹诺酮类药物是一类完全由人工合成的抗菌药物。从1962年偶然发
现第1个喹诺酮类药物—萘啶酸距今已近50年,随着新品种的不断问世,
喹诺酮类药物已经成为临床最为常用的抗感染药物之一,粗略估计,全
球已有超过8亿人接受过喹诺酮类药物的治疗。
早期合成的喹诺酮类药物以萘啶酸、吡哌酸为代表,抗菌谱仅限于
革兰阴性肠道杆菌,对铜绿假单胞菌和革兰阳性球菌无抗菌活性,而且
血药浓度低、组织穿透力差,因此,临床上仅限于尿路感染和肠道感染
的治疗。
20世纪70年代中期,随着氟甲喹的问世,人们开始尝试通过修饰喹
诺酮类药物的基本化学结构来改善这类药物的抗菌活性,喹诺酮类药物
从此进入了一个新的发展时期。从20世纪70年代后期到90年代初,诺氟
沙星、培氟沙星、环丙沙星、氧氟沙星、氟罗沙星、洛美沙星及依诺沙
星等氟喹诺酮品种相继问世。与萘啶酸、吡哌酸等早期合成的品种相比,
上述药物对革兰阴性杆菌的抗蔺活性进一步增强,部分品种对铜绿假单
胞菌也有较好的抗菌活性,同时,由于血药浓度的提高和组织穿透力的
明显改善,这些品种的临床适用范围也不再局限于尿路感染和肠道感染,
也开始广泛应用于包括呼吸系统感染在内的自身各系统的感染。环丙沙
星的成功合成和上市是这一时期喹诺酮类药物研发所获得的最重要的研
究成果,作为第1个可以经静脉滴注全身应用的喹诺酮类药物和具有最强
抗假单胞菌活性的喹诺酮类药物,环丙沙星目前在抗感染治疗中仍然具
有非常重要的应用价值。
20世纪90年代后,左氧氟沙星、加替沙星、莫西沙星及吉米沙星等
品种相继投入临床应用。在体外抗菌活性方面,虽然这些品种对革兰阴
性杆菌的抗菌活性并不优于环丙沙星,但对肺炎链球菌、厌氧菌以及肺
编辑版word
炎支原体、肺炎衣原体、嗜肺军团菌等非典型致病原的抗菌活性却显著
增强(左氧氟沙星对厌氧菌的抗菌活性较弱),能够比较全面地覆盖社区获
得性呼吸道感染的常见致病原;在药代动力学方面,这些品种在肺组织
和呼吸道分泌物中的药物浓度明显高于环丙沙星,而且半衰期更长、口
服剂型的生物利用度更高。由于这些新的氟喹诺酮类药物在抗菌活性和
药代动力学方面能够较好满足社区获得性下呼吸道感染的治疗需要,因
此常被统称为“呼吸喹诺酮类药物”[6-7]。
近年来,喹诺酮类药物的研发进入了一个相对缓慢的时期,但是通
过对喹诺酮母核的改变仍然发现了一些有临床应用价值的品种。研究结
果表明,以加雷沙星为代表的6位去氟喹诺酮类药物(des-F6-quinolone)以
及母核中含有顺式氟环丙胺基团的西他沙星(sitafloxaein)对革兰阳性球菌
的抗菌活性均优于既往已经上市的氟喹诺酮类药物,对某些耐其他氟喹
诺酮类的临床菌株也有良好的杀菌作用[8,9]。重要的喹诺酮类药物的上市
时间见表1。
表1重要的喹诺酮类药物的上市时间表
上市时间
1960-1970年
1970-1980年
1980-1990年
1990-2000年
品种名称
萘啶酸
吡哌酸
氟甲喹
希诺沙星
诺氟沙星
氧氟沙星
环丙沙星
依诺沙星
替马沙星
司帕沙星
左氧氟沙星
格帕沙星
说明
第1个喹诺酮类药物于1962年发现,1964年首先在美国上市,
1967年开始临床应用
1974年发现,1975年上市
第1个单氟喹诺酮类药物,于1976年发现,目前仅限用于畜牧
养殖业
1980年首先在美国上市
第1个可供临床使用的氟喹诺酮类药物,于1978年发现,1984
年首先在日本上市
1985年首先在日本上市
第1个可静脉给药的氟喹诺酮类药物,于1983年发现,1986年
首先在菲律宾上市
1986年首先在日本上市
1992年在英国和美国上市,同年因溶血性贫血、肝肾损害、
低血糖退市[12-13]
1993年首先在日本上市,1995年因严重光毒性在法国被严格
限制适应证[13]
1994首先在日本上市
1997年美国食品药品监督管理局(FDA)批准在美国上市,
1999年因心脏不良事件在美国退市[10]
编辑版word
曲伐沙星
克林沙星
1997年首先在美国上市,1999年因严重肝毒性被美国FDA严
格限制使用,同年欧州药品局建议终止其上市授权[12-13]
1999年因严重光毒性和低血糖撤回上市申请[14-15]
1999年首先在美国上市,2006年因血糖代谢紊乱和心脏不良
事件,百时美施贵宝公司主动终止相关市场活动,同时美国
FDA宣布不再接受口服或注射用加替沙星的其他上市申请
[16]
1999年首先在德国和美国上市
2002年首先在日本上市
2002年首先在韩国和新西兰上市
2007年日本上市
2008年日本上市
加替沙星
2000年至今
莫西沙星
帕珠沙星
吉米沙星
加雷沙星
西他沙星
二、喹诺酮类药物的临床应用现状及存在的问题
(一)喹诺酮类药物的临床应用现状
早期研发的喹诺酮类药物因受抗菌谱、药代动力学及安全性方面的
限制,临床应用范围非常局限,在抗感染药物中所占比例很小。随着环
丙沙星、左氧氟沙星等氟喹诺酮类药物的上市,其抗菌谱广、组织穿透
性强、给药方便、过敏反应少(用药不需要皮试)等优势逐渐显现出来,在
临床上被广泛用于治疗呼吸道感染、皮肤软组织感染、骨关节感染、
腹腔感染、鼻窦炎、泌尿生殖系感染及肠道感染等各系统感染性疾病,
成为抗感染药物中增长最快的一类药物。目前。喹诺酮类药物已经成为
全球销量仅次于B-内酰胺类抗生素的第2大类抗感染药物。在我国,喹诺
酮类药物的销售额已经多年稳居抗感染药物的第2位[10],且一直以年平均
超过10%的速率快速增长。环丙沙星曾经多年高居国内喹诺酮类药物用
量的首位,但随着“呼吸喹诺酮类药物”的相继上市,其所占比例近年
来呈逐渐下降趋势。与此相反,“呼吸喹诺酮类药物”的用量却快速上
升,全国690家医院2006年第2季度的用药分析报告显示,有两种喹诺酮
类药物进入了药品销售额的前20位,其中左氧氟沙星的销售额居所有药
品的第6位和抗感染药品的第3位,加替沙星的销售额居所有药品的第10
位和抗感染药品的第4位,而环丙沙星已经退出药品销量的前20位[11]。
(二)喹诺酮类药物临床应用中存在的问题
1.由于毒性及不良反应和药物相互作用造成的药物安全性问题:喹
编辑版word
诺酮母核的结构简单,比较容易通过改变其分子结构来获得新的品种,
所以喹诺酮类药物一直是近年来发展最快的抗感染药物。粗略统计,自
萘啶酸发现以来,正式注册的喹诺酮类化合物超过了1万种,但真正进入
临床的品种却屈指可数,造成这种高淘汰率的一个重要原因就是毒性及
不良反应。事实上,即使在进入临床研究阶段或已经上市的喹诺酮类药
物中,也一直不断有因毒性及不良反应而终止临床研究或退出市场的品
种(表1)。目前仍在临床应用的品种中,严重的毒性及不良反应和药物相
互作用也屡有报道。
2.致病菌耐药性的快速发展问题:20世纪90年代初,环丙沙星刚刚在
国内上市时,我国大肠埃希菌对环丙沙星的耐药率只有3%左右,到2l世
纪初,我围大肠埃希菌对环丙沙星的耐药率已高达50%,个别地区甚至
超过了70%[17-19]。近年来,世界其他地区大肠埃希菌对喹诺酮类药物的敏
感度也呈下降趋势,根据TEST监测2004--2006年的调查结果,亚太和拉
美地区大肠埃希菌对左氧氟沙星的敏感度已降至70%以下,北美和欧洲
地区大肠埃希菌对左氧氟沙星的敏感度也不到80%[20]。大肠埃希菌等细
菌对喹诺酮类药物存在显著的交叉耐药是此类药物的缺陷之一。
2000--2001年的全国性革兰阴性杆菌耐药性监测结果显示,尽管当时司帕
沙星、加替沙星、莫西沙星等药物尚未在国内投入临床应用,但大肠埃
希菌对这些药物的敏感度均不到50%,与已经在我国临床应用多年的环
丙沙星相当[18]。
3.临床工作中的不合理使用问题:已上市的喹诺酮类药物普遍具有
过敏反应少、给药方法简便等特点,因此许多品种临床应用十分普遍,
但不合理用药现象也比较突出:用药指征掌握不够严格,如外科手术中
的预防性应用和急性上呼吸道感染治疗中的不当使用;忽视或不熟悉喹
诺酮类药物品种间的差别,对品种的选择比较随意;疗程和用药剂量不
当,不合理的长疗程用药现象比较普遍;对喹诺酮类药物的毒性及不良
反应和药物相互作用缺乏警惕性,导致用药风险增加。
4.非医疗性滥用问题:我国畜牧业和水产养殖业中喹诺酮类药物的
滥用情况比较严重,突出地表现为用量大、品种多、使用范围广,町能
编辑版word
是导致我国细菌耐药性快速发展的主要原因之一。
5.临床应用研究薄弱:我国喹诺酮类药物的临床应用研究水平与欧
美发达闰家相比还有较大差距。以环丙沙星和左氧氟沙星为例,欧美多
数国家近年来已经根据药代动力学/药效动力学(PK/PD)理论和相关的
循证医学研究成果对其用药剂量和给药方案进行了修正(环丙沙星
400mg,1次/8h,左氧氟沙星750mg,1次/d)[21]。因为对于新的用药剂量
和给药方案的有效性和安全性缺乏基于我国人的循证医学研究证据,
我国目前仍在沿用传统的用药剂量和给药方案。此外,某些因严重毒性
及不良反应在国外已经被严格限制适应证或退出市场的品种,因多种原
因目前仍然在我国广泛使用。
三、喹诺酮类药物的抗菌机制和耐药机制[22-26]
喹诺酮类药物通过与细菌的DNA解旋酶和拓扑异构酶Ⅳ结合,干扰
细菌细胞的DNA复制而呈现杀菌作用。一般而言,在革兰阴性杆菌中,
喹诺酮类药物作用的首要靶位是DNA解旋酶;而在革兰阳性球菌中,作
用的首要靶位则是拓扑异构酶Ⅳ。但在新开发的喹诺酮类品种中也有一
些例外,如司帕沙星和那地沙星在革兰阳性球菌中对DNA解旋酶的亲和
力明显强于拓扑异构酶Ⅳ,而莫西沙星和克林沙星在革兰阳性球菌中对
DNA解旋酶和拓扑异构酶Ⅳ均具有相似的亲和力。
迄今为止,由染体突变所导致的作用靶位变异和药物摄入减少(细
菌外膜通透性降低或药物主动外排增加)仍然是喹诺酮类药物耐药的主
要原因。在临床分离到的喹诺酮类耐药菌株中,作用靶位变异和药物主
动往往同时存在。事实上,在缺乏主动外排系统的大肠埃希菌中,单纯
的作用靶位变异很少导致喹诺酮类药物MIC值的明显增加。近年来,质
粒介导的喹诺酮类药物耐药开始在临床分离菌株中出现,使喹诺酮类药
物的耐药形势变得更加严峻。尽管这种质粒介导的耐药机制单独存在时
只会导致细菌对喹诺酮类药物产生低水平耐药,但当细菌同时存在作用
靶位变异、外膜通透性下降或主动外排增加等其他喹诺酮类药物耐药机
制时,这种质粒介导的耐药机制可进一步增强细菌对喹诺酮类药物的耐
药水平。
编辑版word
四、喹诺酮类药物的药理学特点
(一)喹诺酮类药物对呼吸道常见致病原的体外抗菌活性
1.革兰阴性杆菌[4-7,17-19,27-28]:喹诺酮类药物对流感嗜血杆菌普遍具有
较好的抗菌活性,临床中对喹诺酮类药物耐药的流感嗜血杆菌目前还非
常少见。对肠杆菌科细菌而言,氟喹诺酮类药物的抗菌活性明显优于早
期上市的非氟喹诺酮类药物,如萘啶酸等品种,但氟喹诺酮类药物的各
品种之间对肠杆菌科细菌的抗菌活性并无实质性差异,新上市的左氧氟
沙星、加替沙星及莫西沙星对肠杆菌科细菌的体外抗菌活性并不优于早
期开发的诺氟沙星和环丙沙星。大肠埃希菌对喹诺酮类药物的高耐药率
是我国特有的现象。从20世纪90年代初至90年代末,在不到l0年的时间里,
我国大肠埃希菌对环丙沙星的耐药率从3%左右升高到了50%以上,个别
地区甚至超过70%,而且各种喹诺酮类药物(包括新一代氟喹诺酮类药物)
之间的交叉耐药现象十分严重。在临床常用的喹诺酮类药物中,环丙沙
星和左氧氟沙星对铜绿假单胞菌的抗菌活性最强,所以也被称为“抗假
单胞菌喹诺酮”[21]。近年来新研发的氟喹诺酮类药物如加替沙星、吉米
沙星、加雷沙星和莫西沙星等对铜绿假单胞菌感染均无临床应用价值。
2.革兰阳性球菌[4-7,17-19,27]:萘啶酸、希诺沙星等早期研发的非氟喹
诺酮类药物对革兰阳性球菌没有抗菌活性。氟喹诺酮类药物对肺炎链球
菌、A族链球菌及甲氧西林敏感的金黄葡萄球菌(MRSA)等革兰阳性球
菌均有一定的抗菌活性。相比较而言,在目前临床常用的氟喹诺酮类药
物中,对肺炎链球菌的体外抗菌活性由强到弱依次为吉米沙星、莫西沙
星、加替沙星、左氧氟沙星、环丙沙星。
3.厌氧菌[4,27-30]:早期研发的萘啶酸等各种非氟喹诺酮类药物无抗厌
氧菌活性。诺氟沙星、氧氟沙星、环丙沙星和左氧氟沙星对厌氧菌的抗
菌活性较弱,后期研发的曲伐沙星、莫西沙星、加替沙星、克林沙星、
加雷沙星及西他沙星等氟喹诺酮类药物均有很强的广谱抗厌氧菌活性,
其中以克林沙星和西他沙星的抗厌氧菌活性最强。但在这屿氟喹诺酮类
药物中,只有曲伐沙星和莫西沙星(仅限于复杂腹腔感染)曾经获得过美国
FDA的批准可用于厌氧菌感染的治疗。
编辑版word
4.非典型致病原[4-7,27]:20世纪90年代以后上市的喹诺酮类药物,如
司帕沙星、左氧氟沙星、加替沙星、莫西沙星、吉米沙星、曲伐沙星、
加雷沙星以及西他沙星等普遍对嗜肺军团菌、肺炎支原体和肺炎衣原体
等非典璎致病原具有很好的抗菌活性。在早期上市的氟喹诺酮类药物中,
环丙沙星和氧氟沙星对非典型致病原也有较好的抗菌活性,但对肺炎支
原体和衣原体属的抗菌活性弱于加替沙星、莫西沙星和吉米沙星。诺氟
沙星和依诺沙星对肺炎支原体和衣原体属的抗菌活性较差。
(二)喹诺酮类药物抗菌作用的PK/PD特征[1-3,31-35]
喹诺酮类药物的杀菌作用呈浓度依赖性,并且具有明显的抗生素后
效应,其体内细菌清除率和临床有效率与AUC[(血清药物浓度-时间)曲线
下面积]
0-24
/MIC、Cmax(最大药物浓度或药物峰浓度)/MIC呈正相关。目
前对于AUC
0-24
/MIC、Cmax/MIC两个指标中哪一个对喹诺酮类药物具有
更好的疗效预测价值尚有争议。考虑到由于药物半衰期和毒性的限制,
某些喹诺酮类药物如环丙沙星不宜采用一日剂量单次给药的方法来提高
Cmax/MIC,因此,目前更倾向于采用AUC
0-24
/MIC来评估和预测喹诺酮
类药物的细菌学疗效和临床疗效。就不同致病菌而言,喹诺酮类药物治
疗肺炎链球菌感染时理想的AUC
0-24
/MIC应达到30-40,治疗革兰阴性肠道
杆菌或铜绿假单胞菌感染时理想的AUC
0-24
/MIC则应达到100以上[11,13]。
就感染严重程度而言,对于轻中度感染患者和(或)无免疫功能缺陷的感染
患者,喹诺酮类药物对致病菌的AU
C0-24
/MIC至少应达到25;对于重症感
染和(或)伴免疫功能缺陷的感染患者,对致病菌的AuC
0-24
/MIC则需要保
持在100以上才能取得理想疗效[4,14]。喹诺酮类药物对呼吸道感染常见致
病菌的总体AUC
0-24
/MIC见表2。必须指出的是,表2中所列AUC
0-24
/MIC
的计算依据是国外的监测数据,考虑到我国大肠埃希菌对喹诺酮类药物
的严重耐药现状,表2中喹诺酮类药物对大肠埃希菌的AUC
0-24
/MIC值町
能并不适合我国的实际情况,仅供参考。
表2规剂量下喹诺酮类药物对呼吸道感染常见致病菌的
AUC
0-24
/MIC(mg·h-1.L-l)
编辑版word
AUC
0-24
/MIC
(全药物)
<12.5
12.5-
25-
50-
niae
依诺沙星
诺氟沙星
环丙沙星
氧氟沙星
左氧氟沙星
司帕沙星
莫西沙星
细菌
nzae
萘啶酸
除萘啶酸外
加替沙星诺氟沙星外
的其他喹诺
吉米沙星
酮类药物
加雷沙星酮类药物
的其他喹诺
萘啶酸
诺氟沙星
除萘啶酸和
nosa
依诺沙星
诺氟沙星
司帕沙星
莫西沙星
加替沙星
吉米沙星
加雷沙星
依诺沙星
氧氟沙星
环丙沙星
左氧氟沙星
>100
表3临床常用喹诺酮类药物的主要药代动力学参数
药物
名称
稳态
治疗方法Cmax
(mg/l)
编辑版word
AUC
0-24
(mg•h-1.
L-l)
生物利半衰期蛋白结清除途
用度(%)(h)合率(%)径
依诺沙星
a
0.5g,1次/12h口服1.519.0ND260肾
诺氟沙星
a
0.4g,1次/12h口服1.510.030-40315肝肾
环丙沙星
b
0.75g,1次/12h口服
0.4g,1次/8h静脉滴注
0.4g,1次/12h口服
3.6
4.1
4.6
31.6
32.9
61.0
70b
98
4
4-5
20-40
32
肝肾
肾
氧氟沙星
b
左氧氟沙
星b
司帕沙星
b
0.5g,1次/d口服
0.75g,1次/d口服
0.5g,1次/d静脉滴注
0.75g,1次/d静脉滴注
0.2g,1次/d口服首剂
加倍
0.4g,1次/d口服
5.7
8.6
6.4
12.1
1.1
47.5
90.7
54.6
108.0
18.7
99
92
6-8
20
24-38
45
肾
肝肾
莫西沙星
b
健康青年4.548901230-50肝肾
健康老年男性3.8
健康老年女性
4.6
健康青年男性
3.6
健康青年女性
4.2
健康青年男性
4.2
健康老年
6.1
4.2
4.6
51.8
54.6
48.2
49.3
0.4g,1次/d静脉滴注38.0
加替沙星
b
48.2
0.4g,1次/d口服
0.4g,1次/d静脉滴注
34.4
35.4
967-1420肾
肾及其
它途径
吉米沙星
b
0.32g,1次/d口服1.69.971760-70
编辑版word
加雷沙星
c
0.4g,1次/d口服7.4100.7ND12.479
肾及其
它途径
注:a数据来自AnderaeonMI,MacGowanAP.JAntimicrobChemother,2003,51:sl-sll;b数据来自
c美国食品药品监督管理局批准的相关药品说明书[38-46];数据来自TakagiH,TanakaK,TsudaH,
.JAntimicrobAgents,2008,32:468-474;ND:没有计算;空白:没有数据
(三)喹诺酮类药物的药代动力学参数[4,8,36-44]
临床常用喹诺酮类药物的主要药代动力学参数见表3,血浆和肺组织
中的浓度见表4。与早期上市的萘啶酸、依诺沙星、诺氟沙星等品种相比,
近年来新上市的莫西沙星、加替沙星、左氧氟沙星和加雷沙星等药物(吉
米沙星除外)的血浆峰浓度更高、AUC更大,具有更为优秀的PK/PD特征,
而且半衰期更长,适宜日剂量单次给药。环丙沙星的半衰期只有4h,明显
短于上述4种新氟喹诺酮类药物,在采用每日0.4g的传统剂量时,血浆浓度
很低,口服日剂量增大至1.5g(0.75g,2次/d)或静脉滴注日剂量增大至1.2
g(0.4g,1次/8h)才能接近上述4种药物的血浆峰浓度。就组织穿透性而言,
呼吸喹诺酮类药物的肺泡上皮衬液浓度(吉米沙星除外)和肺泡巨噬细胞
浓度均明显高于环丙沙星(表4)。
表4临床常用氟喹诺酮类药物在血浆和肺组织中的浓度[6](mg/l)
药物名称
环丙沙星a
加替沙星b
吉米沙星c
左氧氟沙星d
血浆浓度
1.9±0.16
3.22
(2.10-4.50)
1.40±0.44
4.1
肺泡上皮
衬液浓度
3.0±1.05
6.16
(1.70-18.3)
2.69±1.96
10.9
肺泡巨噬
细胞浓度
13.39±3.53
77.32
(48.9-138.5)
107±77
27.7
莫西沙星e3.220.756。7
a注:数据来自Lode,icrobChemther,2002,50:151;250mg,2次/d,连续4d,支气
bc管镜检查时间平均为末次给药后288min;单剂400mg,支气管镜检查时间为给后4h;单剂320mg;
de单剂500mg,支气管镜检查时间为给药后4h;单剂400mg,支气管镜检查时间为给药后2.2h;括
号内为浓度范围。
(四)优化喹诺酮类药物给药方案的思考[1-3,31-35]
根据喹诺酮类药物的PK/PD特征,从药代动力学角度考虑,理想的
给药方案是每日剂量单次给药,以达到最高的血浆Cmax和Auc
0-24
。目前,
新上市的喹诺酮类药物如莫西沙星、加替沙星、吉米沙星大多采用该方
编辑版word
案,左氧氟沙星每日剂量单次给药的方案在国外也得到了普遍接受。与
这些新的氟喹诺酮类药物相比,较早上市的喹诺酮类品种如环丙沙星目
前并未采用每日剂量单次给药方案,一方面是因为半衰期太短(4h),单次
给药无法保证获得理想的Auc
0-24
,而顾虑单次大剂量给药的毒性反应也是
重要原因之一。
就药物剂量而言,目前国内对环丙沙星和左氧氟沙星均采用0.4/d的
剂量。按照PK/PD理论,这种剂鼍无论是对肺炎链球菌还是对革兰阴性
杆菌均不可能获得理想的AUC/MIC和Cmax/MIC,并且很容易将致病菌长
时间置于耐药突变选择窗之内,进而导致耐药突变菌株的选择性增殖和
流行,所以近年来国外已经提高了左氧氟沙星和环丙沙星的日推荐剂量,
在ATS2005年颁布的医院获得性肺炎(HAP)、呼吸机相关性肺炎(VAP)和
医疗卫生相关性肺炎(HCAP)诊治指南中,左氧氟沙星和环丙沙星的日推
荐剂量分别达到了0.75g/d和1.2g/d。考虑到药物代谢的人种间差异,目
前迫切需要对这种大剂量给药在我国人中的安全性做出准确评价。
(五)喹诺酮类药物的防耐药变异能力[44-45]
耐药性的快速发展是喹诺酮类药物临床应用中面临的一个重要问
题。近年来新发展起来的防耐药突变浓度(mutantpreventionconcentration,
MPC)理论为评价和预测喹诺酮类药物对耐药突变菌株的选择性富集能
力提供了新的思路。MPC是指抑制第一步或下一步耐药突变株生长所需
的最低抗菌药物浓度,当药物浓度高于MPC时,病原菌必须同时发生2
次或更多次耐药突变才能生长,因此MPC代表一个严格限制耐药突变株
选择的抗菌药物浓度阈值。按照MPC理论,抗菌药物对耐药突变菌株的
选择能力主要取决于MPC与MIC间的浓度差范围(即耐药突变选择窗,
MSW)和感染部位的抗菌药物浓度,只有抗菌药物浓度在病原菌的MSW
之内时,耐药突变株才会被选择性富集扩增。结合药物的耐药突变选择
特点、现有推荐剂量、Cmax以及半衰期等药代动力学特征,呼吸喹诺酮
类药物在治疗肺炎链球菌感染时,导致耐药突变株选择性增殖的风险按
由大到小的顺序排列,依次为左氧氟沙星、加替沙星、吉米沙星、莫西
沙星。但MPC及MSW特性优异的药物是否确实不易产生耐药,还需长期
编辑版word
的临床研究结果证实。
五、喹诺酮类药物临床应用中的安全性问题[1,10-13,46-50]
(一)喹诺酮类药物的不良反应(表5)
表5喹诺酮类药物的不良反应[1,10-13,46-50]
不良反应
生殖毒性
药物名称
所有药物
氟罗沙星、司帕沙
胃肠道反应
星、格帕沙星除上
述药物以外的其
他品种
皮肤反应
司帕沙星、氟罗沙
光毒性
星、洛美沙星除上
述药物以外的其
他品种
皮疹
软骨毒性
克林沙星
吉米沙星
培氟沙星
除培氟沙星外的
其他品种
4
2.8
14
1.5(接受环丙沙星治疗的儿
童)
年轻妇女
儿童、孕妇
年龄>60岁的老年人,接受糖
皮质激素治疗者,接受肾、心
脏或肺移植者,运动员或从事
肌腱炎培氟沙星2.7
剧烈活动者。2008年7月美同
FDA要求所有上市的全身应
用的氟喹诺酮类药物增加黑
框警告。提示肌腱炎和肌腱断
裂的风险
头呈
头痛
意识障碍或
除培氟沙星外的
其他品种
曲伐沙星
曲伐沙星
左氧氟沙星
0.4(左氧氟沙星/氧氟沙星>
环丙沙星>其他)
2-11
1-5
0.03
老年人
同时使用非甾体类抗炎药
>10
<2.5
囊性肺纤维化
>10
2-8
不良反应发生率(%)
无数据
高危人
孕妇
编辑版word
精神异常(NSAID)或CYP450酶抑制
剂的人
失眠、焦虑氟罗沙星8
癫痫病史、脑外伤、低氧血症、
抽搐所有品种少见联用NSAID,联用茶碱(环丙
沙星、依诺沙星)
心血管系统
毒性
司帕沙星(9-28ms
格帕沙星(10ms)女性及老年患者,联合使用其
延长Q-T间期的药物,联合使
2.9用CYP450抑制剂,有心脏基
础疾病,低钾或低镁血症,肾
功能不全
Q-T间期延
长
莫西沙星(6ms)
左氧氟沙星3ms
加替沙星2.9ms
吉米沙星2.6ms
尖端扭转
室速(Tdp)
司帕沙星
14.5/100万(1999年美国FDA
报告)
1999年因严重心脏事件退出
格帕沙星市场,在报告的7例死亡病例
中3例出现Tdp
1997-2003年美国FDAAERS
系统报告了与左氧氟沙星相
左氧氟沙星
加替沙星
莫西沙星
关的Tdp47例,与加替沙星相
关的Tdp33例,与莫西沙星相
关的Tdp18例,与环丙沙星相
关的Tdp2例。环丙沙星被认为
是目前发生严重心脏不良事
件最少的氟喹诺酮类药物
肝毒性
一过性肝酶
升高
严重肝毒性
格帕沙星
其他品种
曲伐沙星
12-16
<3
0.006
1999年在美国上市18个月后
编辑版word
疗程大于14d
报告了140例严重肝损害病
例,美国FDA因此对其使用范
围进行了严格限制,同年欧
州药品局EMEA建议终止其
上市授权
自发不良反应报告系统10年
莫西沙星
回顾分析,全球发现了8例可
能与使用莫西沙星相关的严
重肝损害
影响血糖稳
定
低血糖加替沙星
克林沙星
左氧氟沙星
莫西沙星
所有人:
<65:<0.1
65-79岁:0.2
高血糖加替沙星
≥80岁:0.6
糖尿病患者
<65岁:1.0
65-79岁:1.6
≥80岁:3.3
血液系统性
溶血
血小板减少
吉米沙星
替马沙星
1.4
0.02(1992年因此退市
接受口服降糖药的高龄
1.7
4(1999年因严重低血糖撤回
上市申请)
1.9
0.65
联用口服降糖药
联用口服降糖药
联用口服降糖药
联用口服长糖药
注:尖端扭转性室性心动过速;中枢神经毒性:总体发生率为1%-2%,按发生风险大小排序
依次为氟罗沙星、曲伐沙星、格帕沙星、诺氟沙星、司帕沙星、环丙沙星、依诺沙星、氧氟沙星、
培氟沙星、加替沙星、吉米沙星、左氧氟沙星及莫西沙星。
喹诺酮类药物总体上是一类比较安全的药物,其最常见的不良反应
为胃肠道反应和中枢神经毒性,绝大多数情况下表现比较轻微,不需要
中断治疗。在已经上市的喹诺酮类药物中,因不良反应而终止治疗的比
编辑版word
例大约为4%。
少见但严重的不良反应包括Q-T间期延长、TdP、肌腱断裂、血糖异
常、肾功能不全、药物性肝炎或肝坏死、溶血、嗜酸细胞性肺炎和抽搐
等,其中Q-T间期延长、TdP、肌腱断裂、血糖异常、药物性肝炎等严重
不良反应往往容易发生在一些特殊的高风险人中,在使用喹诺酮类药
物前应注意仔细识别。
值得注意的是,一些在欧美国家因为严重不良反应而退出市场或限
制使用的喹诺酮类药物目前仍然在国内广泛使用,临床医生在使用前应
熟悉这些药物的严重不良反应,并审慎评估使用这些药物的利弊。
应当强调的是,近年来虽然常有喹诺酮药物导致严重甚至致死性毒
性及不良反应的报告,但整体上发生率极低,考虑到全世界已有超过8
亿人应用过喹诺酮类药物,可以说已上市多年尚未退市或尚未被限制使
用的喹诺酮类药物基本上是安全的。
(二)喹诺酮类药物与其他药物的相互作用。
1.经细胞素酶CYP450途径代谢的药物:多数喹诺酮类药物对细胞
素酶CYP450有不同程度的抑制作用,可以导致与其同时使用的其他经
CYP450途径代谢的药物代谢速度减慢、血药浓度升高。喹诺酮类药物按
照对CYP450抑制能力的强弱排序依次为依诺沙星、克林沙星、环丙沙星、
洛美沙星、氧氟沙星、左氧氟沙星、司帕沙星、加替沙星和莫西沙星。
具体而言,依诺沙星或环丙沙星与环孢霉素同时使用时,可导致后者血
药浓度升高,从而加重免疫抑制和肾毒性,临床中应尽量避免喹诺酮类
药物与环孢霉素等免疫抑制剂联用,必须联用时应监测免疫抑制剂的血
药浓度。依诺沙星与茶碱同时使用时可以导致后者血药浓度成倍增加,
环丙沙星也可导致茶碱的血药浓度增加20%左右,临床中应尽量避免茶
碱与依诺沙星或环丙沙星联用,必须联用时应调整刺量并监测茶碱的血
药浓度,氧氟沙星、洛美沙星、司帕沙星、曲伐沙星以及目前临床使用
的4种呼吸喹诺酮类药物则对茶碱血药浓度的影响很小,无需减少剂量。
依诺沙星或环丙沙星与华法林同时使用时可以增强后者的抗凝作用,并
增大出血风险,必须联用时应加强凝血国际标准比值(INR)的监测。加替
编辑版word
沙星与洋地黄类药物同时使用可以导致后者血药浓度升高,必须联用时
应加强地高辛的血药浓度监测。
2.口服降糖药:喹诺酮类药物与口服降糖药联用时可导致严重的低
血糖或高血糖,必须联用时应加强血糖监测。
3.非甾体类抗炎药(NSAID):喹诺酮类药物与NSAID联用可增加中枢
神经系统不良事件的发生率,临床上主要表现为失眠、精神紧张和抽搐,
应尽量避免联用。
4.抗心律失常药物:喹诺酮类药物与I-A类或Ⅲ类抗心律失常药物联
用时可增加Q-T间期延长的风险,严重时可导致致命性心律失常,应尽
量避免联用。
5.西沙比利:喹诺酮类药物与西沙比利联用也可以导致Q-T间期延
长,应尽量避免联用。
6.大环内酯类抗生素:大环内酯类抗生索单药使用即可导致Q-T间期
延长,与喹诺酮类药物联用町增加Q-T间期延长和发生致命性心律失常
的风险,不推荐联合使用。
7.含有金属离子的口服药:含有镁、铝、铁、钙、锌等金属离子的
口服制剂均可导致口服喹诺酮类药物的生物利用度和血药浓度大幅度降
低。有文献报道,同时服用含金属离子的药物可使环丙沙星的吸收减少
90%,新的氟喹诺酮类药物受影响的程度相对较小,一般认为,钙离子
制剂对莫西沙星、加替沙星的吸收影响不明显。
六、喹诺酮类药物在下呼吸道感染中的选用原则
(一)社区获得性肺炎(CAP)[6-7,51-54]
1.呼吸喹诺酮类药物适用于CAP经验性治疗的重要特点:(1)在抗菌谱
方面,莫西沙星、吉米沙星和左氧氟沙星等呼吸喹诺酮类药物单药即可
同时覆盖CAP常见的致病原。最近完成的2项全国性CAP致病原流行病学
调查结果显示,我国CAP的致病原构成总体上与国外相似,肺炎链
球菌和流感嗜血杆菌仍是CAP最为常见的致病菌,但肺炎支原体的感染
率已超过肺炎链球菌成为我国CAP的首要致病原。此外,细菌与非
典型致病原的混合感染在我国CAP中也占有相当高的比例,在2项调
编辑版word
查中均超过了10%。对肺炎链球菌和流感嗜血杆菌而言,新喹诺酮类药
物的敏感度和体外抗菌活性均优于青霉素和大环内酯类抗生素。我国的
流行病学调杳结果显示,左氧氟沙星、加替沙星和莫两沙星对肺炎链球
菌的敏感度分别为94.2%、94.2%和95.7%,MIC
90
分别为2mg/L、0.5mg/L
和0.25mg/L[18];对流感嗜血杆菌的敏感度分别为100%、96.6%和98.3%,
MIC
90
分别为0.5mc/L、0.25mg/L和0.5nlg/L;对非典型致病原而言,呼
吸喹诺酮类药物对肺炎支原体、肺炎衣原体和嗜肺军团菌的体外抗菌活
性不弱于大环内酯类抗生素,且在吞噬细胞内具有很高浓度,对嗜肺军
团菌的细胞内杀菌作用甚至还要优于大环内酯类抗生素。(2)呼吸喹诺酮
类药物具有适宜CAP治疗的药代动力学特点。就药物的组织分布而言,
呼吸喹诺酮类药物的肺泡上皮衬液浓度远远高于血浆浓度。由于半衰期
长,抗菌作用呈浓度依赖性,每日1次给药即可获得理想的疗效,患者的
依从性较好。此外,此类药物口服剂型的生物利用度很好,可方便轻、
中症CAP患者门诊治疗,也便于序贯性治疗的进行。
2.呼吸喹诺酮类药物在CAP经验性治疗中的应用范围:根据我
国2006年版“社区获得性肺炎诊断和治疗指南”中推荐的经验性治疗方
案[53],呼吸喹诺酮药物可用于青壮年无基础疾病的CAP患者、老年或有
基础疾病的CAP患者、需入院治疗但不必收住ICU的CAP患者以及需要人
住ICU但无铜绿假单胞菌感染危险因素的重症患者,其中后两组患者推
荐采用静脉滴注给药[19]。在2007年美国IDSA/ATS联合发表的CAP指南
中,对于有合并症、免疫功能受损、接受免疫抑制剂治疗、3个月内接受
过其他抗菌药物治疗或存在其他多药耐药肺炎链球菌感染危险因素的门
诊CAP患者以及不需要入住ICU的普通CAP住院患者,也推荐左氧氟沙
星、吉米沙星和莫西沙星等呼吸喹诺酮类药物作为一线治疗药物[20]。此
外,该指南中还特别强调,对于大环内酯类抗生素高水平耐药的肺炎链
球菌菌株已经超过25%的地区应考虑将呼吸喹诺酮类药物作为CAP经验
性治疗的首选[20],这与我国“社区获得性肺炎诊断和治疗指南”中推荐
的经验性治疗方案完全一致[19,53]。
3.除呼吸喹诺酮之外的喹诺酮类药物在CAP治疗中的地位:对于存
编辑版word
在铜绿假单胞菌感染高危因素的CAP患者,具有抗假单胞菌活性的喹诺
酮类药物(环丙沙星或左氧氟沙星)可作为联合用药的一种选择[19-20,53],但
应避免将环丙沙星用于其他无铜绿假单胞菌感染高危因素的CAP患者,
尤其是门诊CAP患者的治疗。其他喹诺酮类药物由于不具有呼吸喹诺酮
类药物在抗菌谱和药代动力学方面的优势,也没有环丙沙星或左氧氟沙
星所具有的抗假单胞菌活性,因此不宜作为CAP经验性治疗的常规药物。
(二)医院获得性肺炎(HAP)[6-7,21,55]
1.无多药耐药菌感染高危冈素的早发性HAP:对于无多药耐药菌感
染高危因素的早发性HAP,初始经验性治疗需要覆盖的主要致病原包括
肺炎链球菌、流感嗜血杆菌、MRSA和非耐药的革兰阴性肠道杆菌,左氧
氟沙星、莫西沙星、加替沙星等呼吸喹诺酮类药物或环丙沙星单药可作
为初始治疗的选择之一,但鉴于我国大肠埃希菌对喹诺酮类药物的高耐
药率,当病原菌已经明确为大肠埃希菌时,除非有药敏试验结果的支持,
原则上不宜选择喹诺酮类药物。
2.迟发性HAP或存在多药耐药菌感染高危因素的HAP:对迟发性
HAP或存在多药耐药菌感染高危因素的HAP患者进行经验性治疗时,除
需覆盖早发性HAP的致病原外,还必须覆盖铜绿假单胞菌、鲍曼不动杆
菌、多药耐药的革兰阴性肠道杆菌、嗜麦芽窄食假单胞菌以及MRSA等多
药耐药细菌。环丙沙星和左氧氟沙星具有较好的抗假单胞菌活性,可与
其他抗假单胞菌药物联用覆盖铜绿假单胞菌,但当病原菌已经明确为大
肠埃希菌时,除非有药敏试验结果的支持,原则上不宜选择喹诺酮类药
物。莫西沙星、吉米沙星对铜绿假单胞菌的抗菌活性并不理想,因此不
宜作为迟发性HAP或存在多药耐药菌感染高危因素的HAP患者的经验性
治疗药物。
(三)慢性阻塞性肺疾病急性加重(AECOPD)[6-7,56-57]
细菌和非典型病原体导致的下呼吸道感染是AECOPD发病的主要原
因之一。近年来的研究结果显示,COPD患者在稳定期气道内已存在细
菌定植,气道内细菌定植可加重气道炎症,在AECOPD时气道内定植菌
浓度明显增加。目前认为,AECOPD患者积极有效地进行抗菌治疗不仅
编辑版word
可迅速缓解患者的症状,而且可有效降低气道内细菌的负荷量,预防下
一次急性加重。AECOPD的初始经验性抗菌治疗需要覆盖的致病原因病
情严重程度和有无耐药菌感染危险因素而不同:轻度加重且无耐药菌感
染危险因素的患者初始治疗时需要覆盖的致病原主要为流感嗜血杆菌、
肺炎链球菌、卡他莫拉菌、肺炎支原体;中度加重、无铜绿假单胞菌感
染危险因素的患者初始治疗时需要覆盖的致病原除前面提到的致病原
外,还包括产酶的流感嗜血杆菌和卡他莫拉菌、青霉素耐药的肺炎链球
菌、革兰阴性肠道杆菌,这两类患者均可选择左氧氟沙星、莫西沙星、
吉米沙星等呼吸喹诺酮类药物单药进行经验性治疗;中重度加重且有铜
绿假单胞菌感染危险因素的患者初始抗感染治疗还必须覆盖铜绿假单胞
菌,因此,一般不宜选用莫西沙星、吉米沙星等药物,但可选用具有抗
假单胞菌活性的环丙沙星或左氧氟沙星与其他抗假单胞菌药物联合进行
经验性治疗。
(此文档部分内容来源于网络,如有侵权请告知删除,文档可自行编辑修改内容,
供参考,感谢您的配合和支持)
编辑版word
推荐内容
-
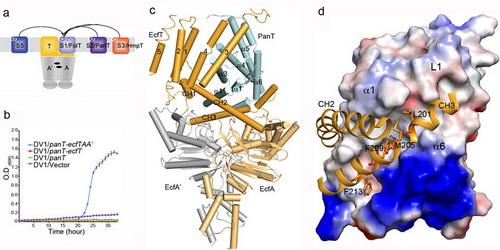
原核转运蛋白有效地转运左撇子和右撇子天冬氨酸
许多生物分子有两个版本,彼此的镜像,如左手和右手。细胞通常使用左手形式的氨基酸来产生蛋白质,并且认为摄取机制共享这种偏好。格罗...
-
中度脂肪肝饮食要注意什么?
-2022年4月20日发(作者:青奥会时间)中度脂肪肝饮食要注意什么?日常,脂肪肝患者要调理好自己的饮食习惯,合理的饮食习惯是很重要的,那么
-
血浆吸附与血浆置换对胆红素清除的效果对比分析
-2022年4月18日发(作者:的副作用)中国医师进修杂志2009年2月5日第32卷第4期 ChinJPoatgradMed,Februar
-
12月6日石家庄疾控疫情最新消息公布 石家庄建议市民非必要不出行
今天石家庄市疫情是什么情况?目前确诊了多少人?今天的你是否在关注石家庄市疫情一事呢?下面跟小编一起来了解下具体详情。今天(12月6日),石
-
中西医结合治疗多囊卵巢综合征验案举隅
-2022年4月24日发(作者:鼻塞)·38·山西中医 2019年3月第35卷第3期 SHANXIJOFTCMMar 2019 Vol 35 No 3·医案医话·中西医结合治疗多囊
-
直接胆红素偏低怎么办
-2022年4月18日发(作者:酒仙桥医院)如对您有帮助,可购买打赏,谢谢直接胆红素偏低怎么办导语:肝功能检查中有直接胆红素这一项,大部分人
-
一个人的墨脱
-2022年4月17日发(作者:茅台镇酒价格表)生活·行憩life本栏目冠名英皇星艺(北京)文化发展有限公司 htsReserved 本刊记者 彭景一个人的墨
-
白芷粉功效作用
-2022年4月18日发(作者:珍珠粉的作用)白芷粉功效作用【白芷粉功效作用】美白祛斑,润肤,控油,延缓皮肤衰老,白芷对美白祛斑有显著的作用,并
-
女生出门定律引热议 看看自己中了几条吧?
网上一则关于女生出门定律 的相关消息引起了网友们的套路,目前这个话题在网络上也是非常火热,小编便从网上搜集了一些相关的信息,下面分
-
8月27日浙江疫情最新数据公布 浙江昨日新增无症状感染者3例
疫情未结束,防控莫松懈。那么,对于浙江疫情的这个话题,今天的你是否也在关注着?下面跟小编一起来了解下具体详情吧。8月26日0-24时,新增