生物物理各章思考题汇总
-
荧光:
1.荧光产生的机理是什么?
P233
(一)荧光的产生
(1)分子的能量状态
在光学分析中涉及的分子能级:
Eo=Ee+Ev+Er
Ee:价电子运动能(电子能级),electron
Ev:原子在平衡位置附近的振动(震动能级),vibration
Er:分子绕其重心的转动能(转动能级),rotation
其中Ee>Ev>Er
(2)分子的能级EnergyLevels与跃迁Transition
2.荧光技术研究的生物学样品的主要参数有哪些?量子产率与荧光强度的区别及关系是
什么?荧光偏振的意义是什么?
P234-237
荧光分光光度术中的参量:
(1)荧光光谱及主要谱参量
荧光光谱包括:镜像对称。
激发光谱(excitatipectrum)(波长:ex——最大激发波长);
发射光谱(emissipectrum)(波长:em,max——最大发射波长)。
(2)荧光强度(fluorescenceintensity,F,I)与量子产率(quantumyield,)
A.荧光强度的定义:在一定激发波长(λex)作用下,发射的荧光强弱。由于发射的荧光为
一光谱,所以发射的荧光强度常常是指发射某一波长的荧光。测得的F不是光能量的绝对
值大小或光子数,而是在一定的仪器条件下测得的一种相对强度。
B.=发射光子数/吸收光子数。表示某种物质的发光本领。任何物质的不会大于1,且同
一物质在不同的环境下,不同。
εεF=Ia,Ia=I
0
-I,I=I
0
10-cL→F=I
0
(1-10-cL)→
→当C很低时F=I
0
εcL→F与C成正比;
→当C较大时F=I
0
→F与C无关。
(3)荧光偏振(fluorescencepolarization)
荧光偏振度Fluorescencepolarization--P=(I
//
-I
)/(I
//
+I
)
荧光各向异性Fluorescenceanisotropy--A=(I
//
-I
)/(I
//
+2I
)
荧光偏振度的物理意义:
A:I
//
=I
,P=0,自然光,荧光分子运动很快,取向随机。(稀溶液)
B:I
//
或I
为0,P=±1,偏振光,荧光分子运动很慢,取向有序。
C:I
//
I
0,0
(4)荧光寿命(fluorescencelifetime--)
荧光衰减为原来激发时最大荧光强度的1/e所需要的时间。
I=I
0
e-kt,=1/k
(5)荧光探针(fluorescenceprobe)
具有环状共轭双键即π电子系统;
量子产率随环境变化,而且变化很大;
能产生稳定荧光的小分子;
藻胆蛋白phycobiliprotein
绿荧光蛋白GreenFluorescentProtein
与研究对象的特定基团共价结合或与蛋白质非共价结合。
3.举例说明荧光技术的应用?
P239-244
4.如果婴幼儿体内缺乏使苯丙氨酸转变为酪氨酸的酶时,则苯丙氨酸的含量异常增大而患
“苯丙酮尿症”且易引起智力低下,所以,对婴幼儿的该项体查极为重要,但是,由于血
液蛋白质中其它芳香氨基酸的影响而难以测出苯丙氨酸的含量,请用本课程所学内容提
出一个检测方案。
P239下-240上
NMR
1题:NMR中外加磁场的作用?
为了使自旋核产生能级分裂而对电磁波产生共振吸收。
2题:.NMR中提高外加磁场的强度的作用?
书247页18-2下边一段,提高外加磁场,增大能级差,以增加分辨率;抵消电子的屏蔽作
用。为了满足共振条件:=H0,即可引起原子核两个能级间的跃迁。共振条件的推导在前
两页。
3题:NMR中如何区分化学位移和J偶合?
理论上讲,同种原子核处于同样的磁场中能级裂分,接受射频时应该在同一位置发生共
振。不同基团中的同种核,因屏蔽不同,造成共振峰位不同,从而产生不同的化学位移。详
见p248。
J耦合是核与核之间以价电子为媒介相互耦合引起谱线分裂的现象,即自旋裂分,见248
页。
化学位移与场强有关,J耦合与场强无关,由基团之间的自旋相互作用引起。通过调节
分辨率可以区分,提高分辨率才会出现的是J耦合。具体见书248、249页。
4题:如何理解NMR中峰宽?
249页第二段,表示物质的量。
蛋白质折叠:
1.蛋白质折叠中的”中心法则”?
生物物理书P22
中心法则:序列结构功能
2.联系生物物理技术部分所学内容,哪些技术可以用来进行蛋白质折叠研究,其根据是什
么?
生物物理书P22-P23
技术:CD:p227-228
红外莱曼:p219
荧光:p240依据:极性对荧光的影响
Nmr:p251依据:化学位移
红外光谱:
1.液态红外光谱是否需要水作溶剂?为什么?
试样中不应含有游离水。在溶液中测定光谱时,由于溶剂的种类、溶剂的浓度和测定时
的温度不同,同一种物质所测得的光谱也不同。通常在极性溶剂中,溶质分子的极性基团的
伸缩振动频率随溶剂极性的增加而向低波数方向移动,并且强度增大。水本身有红外吸收,
会严重干扰样品谱,而且会侵蚀吸收池的盐窗。因此,在红外光谱测定中,应尽量采用非极
性的溶剂。
2.线性分子的振动自由度为什么是3N-5?红外光谱中是否能够观察到所有振动自由度对应
的红外吸收峰?为什么?
设分子由n个原子组成,每个原子在空间都有3个自由度,原子在空间的位置可以用直
角坐标中的3个坐标x、y、z表示,因此,n个原子组成的分子总共应有3n个自由度,即
3n种运动状态。但在这3n种运动状态中,包括3个整个分子的质心沿x、y、z方向平移运
动和3个整个分子绕x、y、z轴的转动运动。这6种运动都不是分子振动,因此,振动形式
应有(3n-6)种。但对于直线型分子,若贯穿所有原子的轴是在x方向,则整个分子只能绕
y、z轴转动,因此,直线性分子的振动形式为(3n-5)种。
每种简正振动都有其特定的振动频率,似乎都应有相应的红外吸收带。实际上,绝大多
数化合物在红外光谱图上出现的峰数远小于理论上计算的振动数,这是由如下原因引起的:
(1)没有偶极矩变化的振动,不产生红外吸收;
(2)相同频率的振动吸收重叠,即简并;
(3)仪器不能区别那些频率十分接近的振动,或吸收带很弱,仪器检测不出;
(4)有些吸收带落在仪器检测范围之外。
例如,线型分子二氧化碳在理论上计算其基本振动数为4,共有4个振动形式,在红外
图谱上有4个吸收峰。但在实际红外图谱中,只出现667cm-1和2349cm-1两个基频吸收
峰。这是因为对称伸缩振动偶极矩变化为零,不产生吸收,而面内变形和面外变形振动的吸
收频率完全一样,发生简并。
基本振动吸收峰数少于振动自由度的原因:
(谱带)简并:不同振动形式的振动频率相同,其吸收峰在红外吸收光谱的同一位置出现。
红外非活性振动:不能引起偶极矩变化(=0),不吸收红外线的振动。
3.CO2的红外光谱中能够观察到几个红外吸收峰?为什么?
两个,一个是反对称伸缩振动的吸收峰,一个是变形振动的吸收峰,本应该有四个,但
对称伸缩振动的偶极矩变化为零,不产生吸收;而变形振动包括面内变形和面外变形,他们
的吸收频率一样,所以重合了。因此只有两个吸收峰.变形:667cm-1伸缩:2369cm-1
4.拉曼光谱中为什么Stokes线的强度远大于反Stokes线?
S是从基态到激发态跃迁,而反S是有激发态到基态跃迁,反斯托克斯线的强度远小于
斯托克斯线的强度,这是由于Boltzmann分布,处于振动基态上的粒子数远大于处于振动激
发态上的粒子数。
CD
1WhenCDisappliedtoproteinswhatisthemainchromophore(absorbinggroup)thatislooked
at?Whatwavelengthrangedoesitabsorbin?当元二光谱应用于蛋白分析时,主要观察哪个
吸收段?主要吸收哪个波段?
主要观察紫外区段,160-300nm
2DoestheCDspectrumofaproteingivemostinformationaboutthe(i)primarystructure,(ii)
secondarystructureor(iii)tertiarystructure?元二光谱主要分析蛋白质的什么信息?主要结
构,二级结构,还是结构?
二级结构,分析蛋白质的二级结构是原二光谱的最基础得应用。
3DrawtheCDspectrumofanα-ertolabeltheaxesandmarkimportantpoints
withtheirvalues.画出α螺旋的图像,注意标记轴和重要点的值。
[]
x
-3E
0
200
21022023024
nm
黄线课本227左下也有
4WhyisnitrogengasusedinCDinstruments?氮气在原二普中的作用?
氮气保护装置
5DoesCDgiveinformationaboutwherethehelicesareinaprotein?应用原二普分析可以了
解蛋白质的螺旋在哪吗?
不能
false?Why?膜蛋白难以用原二普
分析,真还是假?为什么?
膜蛋白是近年来分子生物学研究的热点,膜蛋白是一类具有晶体类似结构的镶嵌于细胞
膜上的蛋白,到目前为止,仅有为数不多的膜蛋白结构得到确认。研究表明,膜蛋白紫外电
子光谱跃迁受到周围环境介电常数的影响,其原因可能是由于溶剂影响了电子由基态跃迁到
激发态(n→π*,π→π*)的跃迁能量。不同于溶液环境中的蛋白质,膜蛋白镶嵌于疏水
的脂质环境之中,因此,膜蛋白紫外CD光谱可能跟溶液状态下的CD信号有所区别。Wallace
等研究表明,以现有的未包括膜蛋白的参考蛋白体系,采用SELCON3、CONTIN及CDSSTR
等拟合运算程序预测具有富含α-螺旋及β-折叠的膜蛋白,其结果与溶液状态的蛋白CD光
谱有差别,特别在190nm后尤为明显;并且溶液状态的CD光谱拟合蛋白结构结果与由
DSSP方法计算的膜蛋白晶体二级结构有差别。所以他们认为,现有的溶液参考蛋白体系不
适合于CD拟合预测膜蛋白二级结构,提倡建立新的含有膜蛋白的参考蛋白体系。
所以可以利用元二谱分析膜蛋白,但要新的参考系。
填空题I
1.脂双层发生凝胶-液晶相转变后,膜流动性增加运动能力加强
2.由于细胞膜的跨膜电位为内负外正所以带负电荷的磷脂趋向分布于脂双层
的内侧
3.X射线晶体学中,结构因子F(S)的物理意义是晶胞中所有电子在方向s的散
射波与单个电子散射波振幅之比,其中含有分子中电子的空间分布(r)的信息
电子密度p(r)可通过F(S)傅里叶变换获得
4.蛋白质跨膜时,肽链必须形成分子内氢键并折叠(α螺旋或β折叠)以
增强疏水性减少极性
5.在功能筏中,分子的运动能力比凝胶态强,比液晶态弱
填空题II
1元素周期表中的过渡金属除锌外均属自由基是因为未配对电子
2自由基的化学活性主要源自孤电子可夺取或失去一个电子配成对
3试举出一种稳定的自由基并说明它的应用
自旋标记物(spinlabels):第一个稳定的化学自由基氮氧化物特点:
应用举例:
报告膜的流动性:将自旋标记物加入到膜脂悬液中时,一部分标记物进入膜内,另一部
分则留在液相,进入膜内的标记物与留在液相的标记物所邻环境十分不同,二者的ESR谱
存在差异。
4试举出自由基对膜脂损伤后膜脂分子常见的几种变化(至少举出两种)
5许多过渡金属的毒性都涉及到活性氧的产生,过渡金属的这一毒性源自
Fenton氏反应
6硫氧环蛋白还原酶的浓度水平常被用来衡量集体的抗氧化应激能力是因为
几乎所有形式的ROS都可以氧化Met为MetO,进而消耗硫氧还蛋白,而Msr可
以把氧化型硫氧还蛋白还原为有活性的硫氧还蛋白
7乙酰胆碱与徐缓激肽对血管舒张作用依赖血管内皮的原因是
其本身无扩血管作用,而需要作用于内皮细胞使其产生NO
8用ESR自旋标记技术测定非顺磁生物大分子的运动情况所依据的主要两点是
答案待定:要考就胡逼答吧!!
1.自旋标记技术(将某些含孤电子的物质——自旋标记物(spinlabels)
连接或掺入到那些本身不具有不成对电子的物质体系中,所纪录到的自旋标记物
的ESR谱能反映与其连接或临近的本身不具有不成对电子的物质体系的某些性
质,使得本身不具有不成对电子的物质体系也可用顺磁共振技术研究现象,此即
为自旋标记技术。许多重要的生物大分子如脂、糖、蛋白等本身并不含有顺磁中
心,正是依靠自旋标记技术,才能够用EPR进行研究获得了关于生物大分子结构、
功能等很多信息。自旋标记技术极大地扩展了EPR技术的应用范围,为EPR技术
的发展作出了重要贡献)
2.不知道答自由基捕获行不?
简答题
简述生物大分子的荧光发光机理及影响荧光强度的因素荧光生团+P232
研究蛋白质二级结构的常用方法有哪些?对于一个结构位未知的蛋白质,请用生
物物理学知识设计一个实验,研究其二级结构,并叙述实验原理P13
试述呼吸爆发的杀菌机制P143
核磁共振的基本原理是什么?为了提高核磁共振分辨率,可以通过提高核磁共振
中外加磁场强度的方法而实现,为什么?P245+思考题
目前认为大脑中蛋白质A贝塔蛋白的聚集是引起老年痴呆的主要原因之一,请应
用本学期所学生物物理学知识并从蛋白质构象变化的角度设计一个体外研究方
案,研究某种药物对老年痴呆是否有一定的治疗作用CD红外蛋白质二级结构
变化
一种双链磷脂的链长为2nm,每条链的直径为0.40nm;该磷脂的头部截面积为
0.50nm2.请用计算说明:该种磷脂与水混合后,以何种聚集状态存在P53
大题:
1.脂质过氧化P155-156
2.计算磷脂分子聚集体状态应用公式s=v/alP53
3.蛋白质四级结构及其意义P21
4.蛋白质二级结构的测定方法,简要介绍其中一种的原理P13
5.生物大分子发生荧光的原理及影响荧光测量的因素荧光生团+P232
6.荧光共振能量转移的三个条件及其应用课件+P241-242
推荐内容
-
肺炎支原体感染致小儿大叶性肺炎21例
-2022年4月22日发(作者:黄鹂鸟吃什么)维普资讯实用医学杂志2008年第24卷第6期 隐静脉曲张87例[J].实用医学杂志,2007,
-
6月17日深圳疫情最新数据公布 深圳新增3例境外输入确诊病例
新冠肺炎疫情对于人们来说,是一场持久的战役。据深圳卫健委通报,6月16日0-24时,深圳新增3例境外输入确诊病例和1例境外输入无症状感染者。
-
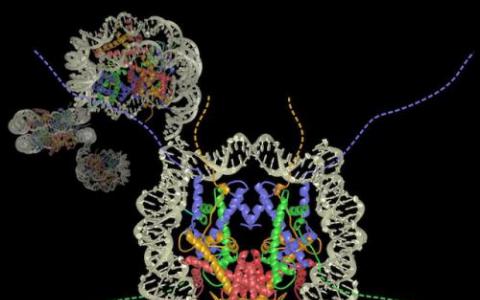
基因调节蛋白的主要家族有药物大小的口袋
称为转录因子的整类蛋白质通过与特定DNA序列相互作用来调节某些基因的活性,但制药行业在很大程度上忽略了它,因为很难设计和筛选针对它们
-
左上腹部疼痛而且嗳气是什么原因
-2022年4月16日发(作者:乙状结肠息肉)如对您有帮助,可购买打赏,谢谢左上腹部疼痛而且嗳气是什么原因导语:有时候我们食用了不干净的食物
-
郑爽我说了算上热搜 具体是怎么回事?
说起郑爽,想必大家都非常熟悉,因为郑爽在观众心目中拥有非常高的地位,深受观众的喜爱。此前有消息称女演员郑爽将接演电影版《花千骨...
-
黄疸治疗方法
-2022年4月18日发(作者:青奥会时间)黄疸治疗方法一、黄疸治疗方法二、婴儿黄疸偏高怎么办三、感染性黄疸怎么办黄疸治疗方法1、黄疸治疗方
-
印度遭遇蝗虫疫情双重灾难 无疑是雪上加霜
说到印度,其实大家的印象应该都是比较落后,环境脏乱的,印度其实是一个经济可以说是很不发达的国家,治安也比较差,印度作为世界第二...
-
8月10日英国疫情最新数据公布 英国昨日新增新冠肺炎确诊病例25161例
大不列颠及北爱尔兰联合王国(英语:The United Kingdom of Great Britain and Northern Ireland),简称英国。本土位于欧洲大陆西北
-
今日美国疫情最新数据公布 美国新增确诊病例7698例
关于美国疫情消息,相信不少小伙伴都一直在关注着。据美国约翰斯·霍普金斯大学发布的全球新冠肺炎数据实时统计系统,截至美国东部时间20...