细胞刚度可能表明癌症转移的可能性
美国,加拿大和中国的工程师和科学家已经开发出一种技术,用于研究实验室生长的3D乳腺肿瘤模型(或类器官)中的细胞的物理特性如何驱动肿瘤成为浸润性的。该团队由麻省理工学院(MIT)工程系的研究人员领导,使用结合了共聚焦显微镜和光学镊子的技术平台,展示了正在生长的乳腺肿瘤类器官内部的细胞如何小而僵硬,而细胞仍在外围较软且肿胀,因为它们包含更多的水。他们的研究表明,这些较柔软的外周细胞如何更能延伸到肿瘤以外并形成“侵袭性尖端”,最终能够分裂并扩散到其他部位或转移。
这些发现为肿瘤细胞的进化和行为提供了新的见解,这些新的见解可能指向新的抗癌治疗策略,这些策略专注于改变癌细胞的物理特性以延缓甚至可能阻止肿瘤扩散。麻省理工学院机械工程学助理教授郭明说:“您可以像海绵一样思考肿瘤。” “当它们长大时,它们会在肿瘤内部建立压应力,这会将水从核心中挤出到外部的细胞中,随着时间的流逝,它们会慢慢溶胀并变软,因此它们更容易侵入。”
包括MIT第一作者Yu Long Han及其同事在内的科学家在《自然物理学》杂志上发表了一篇题为“ 三维乳腺癌模型中的细胞肿胀,软化和浸润 ”的论文,描述了他们的研究结果。
作者解释说,活细胞是经历各种过程的动态系统,包括基因表达,分子水平的细胞内动力学和作用力,以及细胞水平的细胞收缩,变形和迁移。“在多细胞系统中,精确控制时空中的这些物理特性对于维持机械完整性和生物学功能至关重要。”当这种分子和细胞水平出现时,会导致不同的疾病,发育障碍和不良的伤口修复机制不能一起正常工作。研究如何在天然的3D多细胞微环境中维持这些过程是一个真正的挑战,但是迄今为止,
科学家怀疑癌细胞从原发性肿瘤中迁移出来的能力之所以如此,部分原因是它们相对较软且柔韧,从而使它们能够通过人体的血管系统导航至远处。尽管先前的研究已经证明了单个癌细胞的柔软,迁移特性,但Guo的团队开发了一种方法来研究细胞僵硬在3D肿瘤发展过程中的作用。
郭说:“人们长期以来一直关注单细胞,但生物是多细胞的三维系统。” “每个细胞都是物理构建块,我们对每个单个细胞如何调节自身的物理特性感兴趣,因为这些细胞会发展成诸如肿瘤或器官的组织。”
研究人员使用最近开发的技术在实验室中以3D方式生长健康的人类上皮细胞,并将其转化为人类乳腺癌肿瘤。在一周的过程中,研究人员观察了细胞的繁殖并融合为良性原发肿瘤,该肿瘤由数百个单个细胞组成。他们看到了如何从一个细胞开始,一个多细胞簇开始生长,并在大约10天的时间内形成了侵入性分支。
该过程开始于单个细胞的增殖形成球形簇,然后逐渐成长为更大的椭球体,其细胞位于中心或核心,以及边缘或外围。随着球体的进一步发展,侵袭性分支从主体延伸到周围的细胞外基质(ECM)。研究人员说:“在这种3D乳腺癌模型中观察到的表型显示出不受控制的细胞增殖,缺乏细胞极化以及基质浸润的开始,就像在浸润性导管癌中在体内观察到的那样。”
作为实验方法的一部分,研究人员反复向不断增长的细胞团中注入塑料颗粒。然后,他们使用光学镊子探测了每个细胞的硬度。该技术涉及将高度聚焦的激光束对准细胞。在这种情况下,研究小组在每个单元格内的塑料粒子上训练了激光,将粒子固定在适当的位置。然后,他们施加了一个轻微的脉冲,试图在细胞内移动颗粒,类似于使用镊子从周围的蛋黄中挑出一块蛋壳。
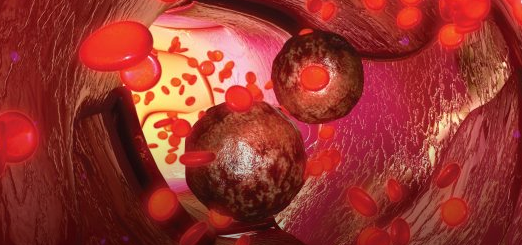
肿瘤的浸润性取决于其水分含量和外部硬度。在第一行中,肿瘤通常朝着侵入性轮廓发展。如果从同一肿瘤(中间排)中抽出水,则与向肿瘤注入水(底部排)时相比,其浸润性较小,从而导致其迅速破裂并侵入周围组织。[于龙涵]
郭说,粒子可以移动的程度表明周围细胞的刚度。粒子移动的阻力越大,细胞必须越坚硬。研究小组的实验结果表明,单个良性肿瘤中的数百个细胞显示出硬度和大小的梯度。不断增长的团块内部的细胞更小,更硬,而细胞离核心越远,它们就越柔软,越大。这些外周细胞也更有可能从球形原发肿瘤中伸出并形成分支或侵入性尖端。
研究人员发现,在肿瘤边缘的细胞比在中心的细胞更柔软,因为它们所含的水分更多。肿瘤中心的细胞被其他向内挤压的细胞所包围,这些细胞通过它们之间的纳米级间隙连接(GJ)通道将水从内部细胞中挤出并进入外围的那些细胞中。
为了观察改变外周细胞的水分含量是否会影响其侵袭行为,研究人员向肿瘤溶液中添加了低分子量聚合物,以将水分从细胞中抽出。他们发现外层细胞随后萎缩,变得更加僵硬,并且不太可能从肿瘤中迁移出来,这是一种延迟转移的措施。当加水稀释肿瘤溶液时,周围的细胞肿胀,变软,并更快地形成侵袭性尖端。
然后研究人员获得了患者乳腺癌肿瘤的样品,并测量了肿瘤样品中每个细胞的大小。他们观察到的大小梯度与实验室衍生的肿瘤相似。肿瘤核心中的细胞比近端的细胞小。科学家指出:“在肿块内,明显可见被基底膜围绕的球形,腺泡状细胞簇,它们与我们的3D癌症模型具有相似的特征。” “在这样的球状腺泡簇中,我们发现随着距中心的距离增加,核体积也增加,这与我们的模型系统一致。核心细胞的体积较小,而似乎已从主簇中逸出的浸润细胞的体积较大。”
郭说:“我们发现这不仅仅是在模型系统中发生,而是真实的。” “这意味着我们可能能够根据实际情况开发一些治疗方法,以确定细胞的硬度或大小,看看是否有帮助。如果使细胞变硬,它们迁移的可能性就会降低,这可能会延迟入侵。”
作者指出,间隙连接在癌症进展中的作用尚有争议,“在各种类型的癌症和GJ中都观察到了侵袭性的促进和抑制。”他们认为,其结果暗示着纯粹的物理机制。 GJ可以影响癌症的进展。“细胞含水量的变化以及因此分子拥挤的程度将影响下游细胞的广泛功能和特性……这些机械变化显示为通过间隙连接的细胞上液流动引起的,抑制这种行为会延迟细胞的流动。过渡到侵袭性表型……如此,我们对肿瘤进展的新兴物理图像现在包括细胞物理特性的3D时空演化。”
郭认为,未来临床医生可能能够观察到肿瘤,并基于从内到外的细胞大小和刚度,可以有把握地说出肿瘤是否会转移。郭说:“如果存在确定的尺寸或刚度梯度,您会知道这会造成麻烦。” “如果没有渐变,您也许可以放心地说很好。”
推荐内容
-
补肾补气补血的食品种类
-2022年4月16日发(作者:2016奥运会乒乓球比赛)如对您有帮助,可购买打赏,谢谢补肾补气补血的食品种类导语:现代人们不论男性还是女性,都
-
10味中药茶饮巧治失眠
-2022年4月18日发(作者:全民健康网)10味中药茶饮巧治失眠失眠是指经常不易入睡,或睡后易醒,或醒后不能再寐,或睡时多梦,或彻夜不寐的一
-
10月22日甘肃嘉峪关疫情最新消息公布 嘉峪关市第二轮全员核酸检
嘉峪关,号称天下第一雄关,位于甘肃省嘉峪关市西5千米处最狭窄的山谷中部,城关两侧的城墙横穿沙漠戈壁,北连黑山悬壁长城,南接天下第一
-
强直性脊柱炎的功能锻炼
-2022年4月24日发(作者:重庆癫痫病医院)136 2护理配合 内蒙古中医药 病Jh ̄,f2。体位固定以不影响呼吸和血液循环、适应手术为
-
12月4日墨西哥疫情数据消息公布 墨西哥确认境内首例奥密克戎毒株
墨西哥合众国(西班牙语:Los Estados Unidos Mexicanos),简称墨西哥,是北美洲的一个联邦共和制国家,北部同美国接壤,南侧和西侧滨临
-
分子变色龙揭示细菌生物膜
改变颜色的分子可用于实时跟踪细菌如何在其周围形成保护性生物膜。这种新方法由林雪平大学和瑞典卡罗林斯卡医学院的研究人员合作开发,...
-
新的基因治疗方法为解决罕见的遗传性疾病创造了新的途径
无义突变是遗传密码中的单字母错误,过早地停止了关键蛋白质的产生。这些未完成的蛋白质不能正常发挥功能,无义突变导致所有遗传性疾病...
-
治疗咽喉炎见效最快的方法咽喉炎的快速治疗方法
-2022年4月22日发(作者:早泄的)治疗咽喉炎见效最快的方法咽喉炎的快速治疗方法一、病因治疗:清除邻近病灶,治疗全身疾病,戒除烟酒,预防
-
8月29日河南郑州疫情最新实时消息公布 郑州全面恢复市区巡游出租
郑州全面恢复市区巡游出租汽车及网约车运营。那么,对于河南郑州的这个话题,今天的你是否也在关注着?具体什么情况?下面跟小编一起来了...
-
徐文兵解读汇报黄帝内经视频全集(350集视频全面)
-2022年4月16日发(作者:长沙理工大学云塘校区地址)实用文档徐文兵解读黄帝内经视频全集(350集视频最全)徐文兵解读黄帝内经视频全集(350集




