新线索显示失控突触修剪可能位于阿尔茨海默病的基础上
对我们许多人来说,阿兹海默氏病是一种熟悉和可怕的疾病。困扰着美国估计的530万人,这种混乱缓慢而无情的折磨着记忆、判断和感知的病人,最终腐蚀了他们执行日常任务的能力。这些症状所依据的机制还没有得到充分的理解。该疾病主要归因于蛋白质的异常积累,其可在大脑中形成淀粉样蛋白beta斑和Tangles,其引发炎症并导致称为突触的脑连接丧失,其作用与认知下降最强烈相关。

在本周发表在“科学”杂志上的一项研究中,波士顿儿童医院的神经学家贝丝·史蒂文斯领导的一组研究人员发现,这种突触缺失实际上可能在阿尔茨海默病中发生得更早。这一过程可能早在斑块形成之前就开始了,而不是像专家们先前所认为的那样,成为这些蛋白质病理的第二效应。
Synapse消除或“突触修剪,”是在开发过程中发生的一个正常过程,一个Stevens已经被多年的迷住了。她发现了一些能引发免疫反应的蛋白质,以清除任何疾病的先兆,也在标记弱或不想要的突触以消除的作用中发挥作用。这个过程允许专门的pac-man-像所谓的小胶质细胞的脑细胞吞噬靶向突触,为更精确的脑配线铺平道路。
在我们的生活中,大脑的交叉点被修剪和修剪,这是一个对正常发展至关重要的过程。Stevens和她的团队怀疑参与这种修剪的机制可能会被异常地打开--劫持,从而说话---帮助阿耳茨海默氏综合症的突触丢失。“这就是我们面对这个问题的唯一方式,”说.“这个项目引发的许多工作源于我们了解这些途径在正常大脑发育过程中的作用,以及我们更多地了解它是如何正常工作的,我们认为它将为我们提供关于如何在疾病中对其进行治疗的新见解。”
研究人员使用小鼠模型对他们的理论进行了测试,使用了高分辨率成像技术来精确定位何时和何处发生突触丢失。在这种啮齿动物模型中,在斑块出现之前存在时间窗,在此期间研究人员观察到小鼠在海马中失去突触,大脑区域负责记忆和学习。
Stevens注意到,特别引人注目的是,研究人员还发现C1q的高表达,一种参与正常突触修剪的蛋白质。“所以我们想知道:[这些蛋白质]会导致这些模型中的突触丢失吗?”说。研究人员敲除C1q和C3基因(由C1q激活的蛋白质),并发现通过这样做,它们保护了小鼠的突触。
为了更好地解释这一发现,研究小组转向了另一种蛋白质,淀粉样β-它的可溶性形式,在形成并硬化成斑块之前,已经被发现对突触有毒。研究人员将这种毒性形式的淀粉样β交付给三组小鼠:一组正常对照组,一组基因缺乏C1q,另一组用一种阻断C1q在大脑中功能的抗体治疗。在第一组中,广泛的突触丢失发生在海马-在C1q被抑制的小鼠中没有发生这种丢失。史蒂文斯说:“这表明C1Q和淀粉样β在同一条途径上起作用。”“C1q是淀粉样β引起这种损伤所必需的。”利用这一实验模型,研究人员随后观察了小胶质细胞的行为,发现淀粉样β的可溶性形式刺激小胶质细胞吞噬突触。然而,抑制C1q可以防止这种影响。
“本研究是我们了解阿尔茨海默病的分子机制的主要进展,在证明免疫分子在这种疾病中的因果关系时,”说,加州大学戴维斯分校的神经生物学家,没有参与这项研究。“对我来说真的很刺激,”在爱丁堡大学的神经科学家塔拉斯皮尔-琼斯(TaraSpitres-Jones)也未加入这项研究。“这是场的两个部分......突触丧失和炎症问题联系在一起。”
悉尼大学的神经病理学家曼努埃尔•格拉贝尔认为,这些研究结果也将在聚焦科学家“关注这些细胞”功能方面发挥重要作用。他说,这篇文章强调了大脑的这种维持系统,“没有足够的了解,”他说。一般研究人员将这些细胞与免疫反应联系起来;然而,Stevens和她的同事的工作在不同的光中揭示了这些细胞。“我认为这有助于纠正这种误解。”
史蒂文斯的团队认为,他们的结果影响到远远超过阿兹海默氏病的影响。“我们对这样的可能性感到兴奋,即这是一个更全球性的机制,它不是疾病特有的,”Stevens说,由于突触丢失在其他疾病如孤独症、精神分裂症、亨廷顿和青光眼中起着重要作用。她已经开始在其他疾病模型中测试这个想法。
最近一项研究将精神分裂症与基因C4的变异联系在一起也暗示了参与突触修剪的途径。“这些发现提示靶向该途径的新的治疗剂可以治疗广泛的神经变性和精神疾病,”McCallister说。
然而,发展这种治疗在未来仍然是遥远的。研究人员首先需要测试他们在人类中的发现,还有其他因素要考虑。例如,它们还没有确定负责初始切换C1q的机制。Stevens说,这个因素是“可能与很多疾病有关-在上游我们也可以考虑靶向性,”Stevens说的。C1q通过清除死细胞和帮助目标有害物质,在大脑中也起到了积极的作用,因此学习如何操纵其存在以防止衰弱的突触丧失,同时维持其正常功能需要进一步研究。
此外,其他研究小组已经确定了靶向治疗的不同途径。在本周在科学翻译医学上发表的另一项啮齿动物研究中,来自多个机构的一组研究人员确定了形成淀粉样斑块的途径。更具体地,他们发现,在细胞(包括神经元)表面发现的一类分子肝素基本上是“陷阱”淀粉样肽,使它们聚集并形成最终导致神经变性和痴呆的沉积物。当研究小组删除了一个允许肝素钙粘附到神经元表面的基因时,他们发现了更少的淀粉样斑。“而不是使用免疫方法或以具有副作用的酶为目标,我们希望靶向该特异性途径,使得当它们“未被肝素俘获时,脑可以天然地清除淀粉样蛋白-beta肽,”说,佛罗里达州杰克逊维尔梅奥诊所的神经科学家国军BU和研究的首席作者。
同样,Stevens对她对开发治疗的发现的未来效用感到乐观。“C1q似乎是个好目标,”Stevens说,“我们没有证据表明[这些蛋白质]驱动整个过程,但我们认为它是一个早期的部分,如果你把它敲出或操纵它,你就可以有一个早期的影响,至少保护故事的突触部分。”
推荐内容
-
7月28日云南瑞丽疫情最新数据公布 云南新增2例本土确诊病例
提起云南瑞丽,很多人都不太陌生,这个城市位于云南省最西部,和缅甸城市木姐相邻,也是我国一个特殊的边境贸易区。作为我国西南地区知...
-
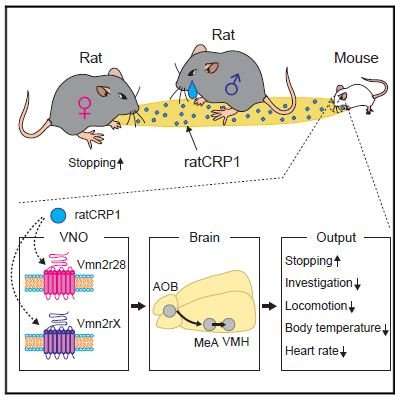
小鼠'窃听'老鼠的泪液信号
眼泪似乎没有气味。但是研究表明,眼泪中的蛋白质确实可以起到信息素的作用。例如,雄性小鼠的泪腺产生一种蛋白质,使女性更容易接受性...
-
第二届北京国际妇科微创诊疗技术学术论坛(GMTC)及北京妇产医院妇
-2022年4月17日发(作者:成都静脉曲张医院)维普资讯2007年9月第45卷第l3期 ・中医中药・ 酸2l7 mo ;B超提示:肝内回声
-
品之减肥食品论文
-2022年4月18日发(作者:莲花山门票)题目:减肥食品——人类的营养补充剂学院:专业班级:姓名:学号:减肥食品——人类的营养补充剂摘...
-
我国疫苗适合快速应对变异 中国疾控中心专家怎么说?
大家都知道,疫苗是防控传染病最有效的手段,中国疾控中心研究员邵一鸣:已经在针对变异株研制新一代疫苗,我们国家灭活疫苗的技术路线...
-
舒适护理在股骨颈骨折护理中的效果
-2022年4月24日发(作者:裂便血)世界最新医学信息文摘2019年第19卷第36期271·护理研究·舒适护理在股骨颈骨折护理中的效果李海芹(山东省
-
基本药物不占药比 基药目录搅动千亿市场
你知道哪些药物属于基本药物吗?而基药目录搅动千亿市场又是怎么一回事?那么都有哪些地方开始实施了呢?让我们跟小编去看看吧!基本药物是安全
-
出血热是传染病?出血热有哪些症状附预防方法!
出血热即流行性出血热又称肾综合征出血热,是危害人类健康的重要传染病,是由流行性出血热病毒(汉坦病毒)引起的,以鼠类为主要传染源的...
-
12月11日绍兴上虞区区疫情最新消息公布 绍兴上虞区:对东关街道
小编在这里提醒大家,疫情期间仍然有一些隐患是不可忽视的,所以在去到一些人流量 大,人员密集度高的环境下时,大家还是要戴好口罩,才能
-
游客爬上日观峰遭其他游客怒骂 真不要脸没素质
今日一则关于游客爬上日观峰遭其他游客怒骂的消息引起了大家的关注,针对此消息,小编整理了相关的资料信息,下面一起来了解下。近日,...