小分子建立安全系统来保护基因组
成千上万具有不同基因序列的短RNA分子可用作识别和沉默侵入基因组的安全措施,例如由病毒插入的DNA或称为转座子的寄生元件。
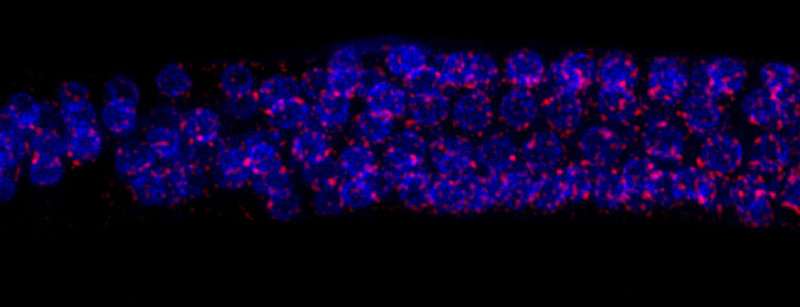
这些多样的小RNA分子,称为Piwi相互作用RNA(piRNA),是由各种动物产生的,从昆虫和蠕虫到哺乳动物如小鼠和人类。在2月2日发表在“科学”杂志上的一项新研究中,芝加哥大学的研究人员描述了piRNA如何找到外来基因序列来使它们沉默。他们还展示了适当属于基因组的内源性或“自我”基因如何识别自身以避免这种额外的审查。
“几乎所有的动物都有这些小RNA,它们用它们作为寻找靶序列并使它们沉默的指南,”UChicago分子遗传学和细胞生物学助理教授,新的高级作者Lee-Chi Lee博士说。研究。“但直到现在,它们的功能是多么神秘,以及为什么有这么多具有如此多样化的基因序列。”
嫌疑人数据库
RNA充当信使,以执行在DNA中编码的指令,以产生在体内执行基本功能的蛋白质。在这项新研究中,Lee和他的同事们研究了线虫蠕虫C. elegans的生殖系统细胞产生的piRNAs,这是科学家研究的经典模式生物,用于理解基本的生物过程。
Piwi相互作用的RNA是一种小RNA,与细胞中的Argonaute机器相关联,可以搜索靶RNA并将其关闭。RNA使用与镜像DNA序列相同的核苷酸链构建,用相同的熟悉的A,C,G,U字母表示。一些小RNA需要精确匹配目标序列以识别它们,就像寻找特定人的保安一样。其他小RNA可以标记部分匹配的基因,更像是根据一般描述寻找嫌疑人。
科学家们并不确定piRNA是如何找到它们的目标的,部分原因是因为它们有很多。例如,Lee研究的线虫具有超过15,000个具有不同核苷酸序列的piRNA。为什么会有这么多,他想知道,他们的目的是什么?
“目前还不清楚为什么细胞必须产生如此多的piRNA。它们如此多样化以至于很难知道哪一种能够识别哪种靶RNA。这种关系过于复杂,”Lee说。
当Piwis识别他们的目标时,他们会招募一组甚至更小的二级RNA,这些二级RNA对应于目标位点的序列,这是一种标记它以引起注意的方式。知道了这一点,Lee和他的团队创建了一个合成的piRNA,其序列在蠕虫中不存在,并跟踪它创建标记的位置。然后,通过检查标记的合成piRNA的不同序列,它们可以向后工作以找出其找到匹配的逻辑。
事实证明,piRNA需要与序列的一部分相当匹配,但它们可以容忍其余部分的一些不匹配。似乎蠕虫中存在许多未配对的Piwis,因为它为它们提供了许多可能的序列组合的工具箱,它们可能需要识别外源RNA并将其关闭。他们拥有一个可能的嫌疑人的完整数据库,而不是寻找特定人员的保安人员,或者他们可以追踪的人。
避免误报
但他们如何避免误报,或者错误地识别属于那里的内源性“自我”基因呢?为了找到答案,Lee和他的同事设计了更多的piRNA,可以识别属于线虫基因组的几个众所周知的基因。但是这组piRNA根本没有沉默或影响内源基因的功能,这意味着它们在某种程度上具有抗性。
研究人员还发现许多内源基因具有额外的A和T核苷酸重复部分,这些部分将其标记为“自我”而非外来的。该许可信号用作识别基因的凭证,用于显示其所属的piRNA系统的护照。
“我们证明了内源基因能够通过许可系统抵抗piRNA系统,这真的很酷,”Lee说。“他们所要做的就是用'自我'信号标记自己。”
该研究揭示了影响动物生育能力的基本机制。以前的研究表明,如果Piwi基因发生突变,piRNA系统就会出现故障。然后,如果病毒或转座子将外源DNA元件注入种系,或产生卵子和精子的生殖细胞,那么piRNA就不能检测和沉默它们。这些未被发现的变化可能导致不育和生殖系统的其他问题。
一个困扰生物学家多年的实际障碍
该研究还解决了几十年来一直困扰秀丽隐杆线虫科学家的技术问题。当研究人员想要研究特定基因时,他们经常会进行轻微修改,因此产生荧光的特殊蛋白质标签可以附着在他们感兴趣的基因产生的蛋白质上。这在大多数类型的细胞中都很有效,但在种系中,piRNA系统发现了这些遗传变化并关闭了荧光标签的产生。
Lee和他的团队展示了科学家们如何防止这种情况发生。通过编辑piRNA识别的位点就足够了,他们再也找不到了它们,但这些基因的功能仍然相同。研究人员还可以将相同的自我许可信号插入DNA的非编码部分,以使变化看起来属于内源基因。这些技术还将允许科学家使用CRISPR-Cas9基因编辑系统来追踪种系的变化。
“当我第一次在一次会议上发表这篇文章时,在我的谈话之后,我被30位科学家请求帮助所包围,所以他们可以使用我们的算法来研究他们自己在生殖细胞中最喜欢的目标,”Lee说。“它解决了过去20年来困扰秀丽隐杆线虫生物学家的一个非常实际的障碍。”
推荐内容
-
如何判断自己能否接种新冠疫苗
-2022年4月21日发(作者:四川理工学院怎么样)XXXX医院如何判断自己能否接种新冠疫苗在疫苗接种现场,我们常常会碰到对接种同意书上的相关条
-
常用中药名大全
-2022年4月18日发(作者:空间个性名字)两字:人参人发卜芥儿茶八角丁香刀豆三七三棱干姜干漆广白广角广丹大黄大戟大枣大蒜大蓟小蓟小麦小蘖
-
忍冬规范化栽培
-2022年4月17日发(作者:孙丹燕)Y u . 冬规范化栽谤 ●张正海李爱民魏盼盼(中国农业科学院特产研究所吉林吉林132109) 金银
-
今日广东疫情最新情况 广东新增本土确诊15例 无症状5例
国内疫情情况的好转,让很多人放松了警惕,大家都以为不会再出现本土病例了,但最近病毒却用行动打了我们一个措手不及6月2日0-24时,全省新
-
苹果下架iPhone 8真的吗?iPhone 8下架后还可以买到吗
近日一则苹果下架iPhone 8的消息,引发大家的热议,许多小伙伴都在问苹果为什么要下架iPhone 8,下架之后还能没得到吗?下面就一起去了解
-
7月19日俄罗斯疫情最新数据公布 俄罗斯新增确诊病例25018例
随着新冠疫情俄罗斯蔓延,新增病例人数持续上升,防控形势不容乐观,据俄罗斯新冠病毒防疫官网18日公布的最新数据,俄罗斯新增新冠肺炎...
-
11月1日银川疫情最新消息公布 银川新增确诊病例活动轨迹公布
想必大家都知道,银川,简称银,是宁夏回族自治区首府,国务院批复确定的中国西北地区重要的中心城市。那么,你知道银川目前疫情什么情...
-
补脾益肠丸说明书
-2022年4月21日发(作者:今天哪地震了)补脾益肠丸说明书请仔细阅读说明书并按说明使用或在药师指导下购买和使用[药品名称]通用名称:补脾益
-
2022年元旦股市放假几天?2022年股票市场休市安排时间表一览
元旦,即公历的1月1日,是世界多数国家通称的新年。元,谓始,凡数之始称为元;旦,谓日;元旦即初始之日的意思。元旦通常指历法中的首月首日
-
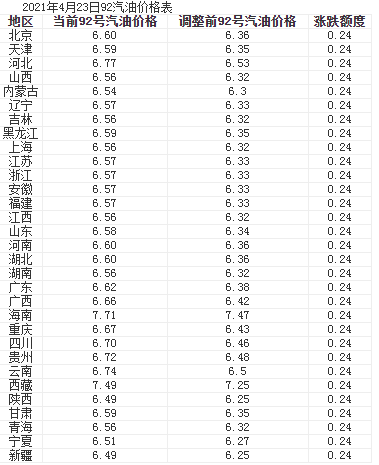
4月23日油价调整最新消息 今日92号汽油价格多少钱一升?
随着社会经济的发展,越来越多的人选择汽车作为出行的代步工具。而对于拥有汽车的你,想必最关注的就是油价这一块了。那么,你知道今日...