科学家改善基因治疗中的DNA转移
帕金森病,亨廷顿病,囊性纤维化和许多其他致命的人类疾病都是遗传性的。许多癌症和心血管疾病也是由遗传缺陷引起的。基因治疗是治疗这些疾病的有希望的可能性。在遗传修饰病毒的帮助下,DNA被引入细胞以修复或替换缺陷基因。通过这种方法,来自德国灵长类动物中心(DPZ) - 莱布尼茨灵长类动物研究所的科学家们发现了一种更快,更有效的细胞治疗方法。科学家改变了用于生产治疗性病毒的所谓HEK293细胞系。然后细胞大量产生一种叫做CD9的蛋白质。此外,他们以这样的方式修饰病毒进行基因转移,即CD9整合到它们的包膜中。这些遗传操作导致靶细胞的更快和更有效的感染。由此导致的DNA向靶细胞的较高转移率有望实现新的和改进的基因疗法治疗。
该研究发表在“分子疗法”杂志上。
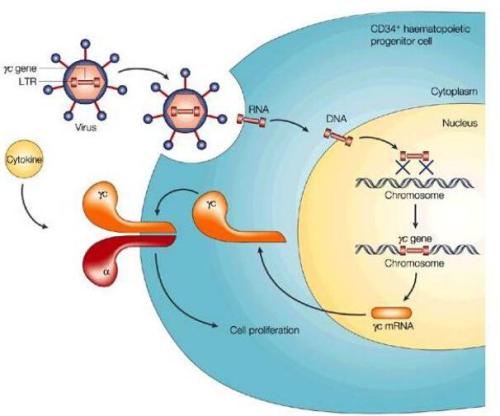
病毒将其遗传物质引入宿主细胞的能力被用作基因治疗的工具。这些“基因出租车”由修饰的病毒组成,即所谓的病毒载体。它们配备了功能齐全的基因,可替代细胞中有缺陷的致病基因。但是,先决条件是病毒识别并感染相应的细胞。
“在我们的研究中,我们想知道是否有可能提高病毒载体的感染率以及如何,”初级研究组组长兼该研究的高级作者Jens Gruber说。“目前,感染率取决于目标细胞,通常约为20%,这对于某些疗法来说还不够。”
为了改变这种状况,研究人员研究了所谓的外泌体的产生,以找出如何使用这种机制以使病毒载体变得更有效。外来体是充满蛋白质,RNA或其他分子的小膜囊泡。它们用于细胞组分的运输和细胞间通讯。“我们的假设是,我们可以通过促进细胞中的外泌体生成来改善病毒的产生及其效率,”Gruber解释了运输囊泡对该研究的相关性。
为了产生大量的CD9蛋白,Gruber和他的团队对用于生产病毒载体的HEK293细胞系进行了基因工程改造。该蛋白质因其在细胞运动,细胞 - 细胞接触和膜融合中的功能而闻名。假设它也可以在外泌体生产中发挥作用。此外,科学家将CD9蛋白掺入病毒载体的包膜中。
“我们能够观察到两件事,”格鲁伯说。“首先,与未处理的HEK293细胞相比,HEK293-CD9细胞中的外泌体产生显着增加,这表明该蛋白质在外来体形成中的关键作用。其次,CD9蛋白质在病毒膜中的掺入显着改善了在没有实施额外病毒载体的情况下,在携带所需基因的感染靶细胞数量增加的情况下观察到这种情况。“
病毒中CD9的量增加导致更高的感染率约为80%。该蛋白质似乎对外泌体产生和病毒效率具有直接影响,这在先前尚未描述过。“我们的研究结果为我们提供了对外泌体形成以及细胞内病毒生成的更好理解,”Gruber说。“这些研究结果可用于使目前使用的基于病毒的基因疗法更有效。未来,我们可能完全避免使用病毒,只使用外泌体将遗传物质转运到靶细胞中。”
推荐内容
-
狗狗咬榴莲被主人训 网友:这样子委屈极了好可爱了
对于狗狗这种生物大家应该是都不陌生的,尤其是最近这两年养狗的人越来越多了,今日,有网友发布了一条自家狗狗的视频,视频中狗狗正捂着鼻
-
7月24日绵阳疫情最新数据公布 绵阳新增1例本土确诊病例
绵阳,别称中国科技城,四川省地级市,位于四川盆地西北部,涪江中上游地带。东邻广元市的青川县、剑阁县和南充市的南部县、西充县;南接遂
-
氟伏沙明合并森田疗法治疗难治性强迫症的疗效分析
-2022年4月20日发(作者:李宗伟退役)2013年10月 中国民康医学 Oct,2013 第25卷上半月第19期 Medical Jou
-
兰州大学专职组织员管理暂行办法试行
-2022年4月24日发(作者:小儿遗尿症)兰州大学专职组织员管理暂行办法(试行)第一条为深入贯彻落实党的十八届六中全会和全国高校思想政治工
-
莲藕:不同部位功效不一
-2022年4月18日发(作者:五倍子的功效与作用)龙源期刊网莲藕:不同部位功效不一作者:来源:《饮食与健康·下旬刊》2014年第09期莲藕属睡莲
-
C罗一动作让可口可乐市值蒸发256亿怎么回事?C罗为什么要挪走桌子
C罗挪走桌上饮料,可口可乐市值蒸发40亿美元是怎么回事?而对于C罗一动作让可口可乐市值蒸发256亿的这个话题,今天的你是否也在关注着?究竟
-
父母50岁还可以贷款30年吗?最多贷款几年呢?
贷款(电子借条信用贷款)简单通俗的理解,就是需要利息的借钱。贷款是银行或其他金融机构按一定利率和必须归还等条件出借货币资金的一种...
-
蛇莲化斑散治疗外阴白斑的案例报告分析
-2022年4月16日发(作者:广西旅游攻略必去景点)中国中医杂志2012年6月第23卷第6期蛇莲化斑散治疗外阴白斑的案例报告分析【摘要】外阴白斑又
-
白岩松对话姚明 姚明说了什么?
对于姚明大家应该是一点都不陌生的,姚明在我们心里应该都是很熟悉的。昨晚(8日),白岩松连线中国篮球协会主席姚明,解读疫情下的中国篮球
-
杨丞琳潘玮柏蔡依林同框 三人的友谊令人羡慕
杨丞琳潘玮柏蔡依林同框的相关消息引起了网上热议,具体是怎么回事,下面跟随小编一起去了解一下吧?5月24日,杨丞琳在社交平台晒出自己和潘




